题目内容
17.如表四个实验方案设计不合理的是( )| 选项 | 实验目的 | 方 案 |
| A | 鉴别KNO3溶液和K2SO4溶液 | 取样,滴加Ba(NO3)2溶液,观察现象 |
| B | 除去NaOH溶液中的Na2CO3杂质 | 加入适量的CaCl2溶液,反应后过滤 |
| C | 除去CaO中的CaCO3 | 高温加热到固体质量不变 |
| D | 区别NaOH和NH4NO3固体 | 分别加入水中溶解,用手触摸烧杯外壁 |
| A. | A | B. | B | C. | C | D. | D |
分析 硫酸钾和硝酸钡反应生成白色沉淀硫酸钡和硝酸钾;
碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;
高温条件下,碳酸钙分解生成氧化钙和二氧化碳;
氢氧化钠溶于水放热,硝酸铵溶于水吸热.
解答 解:A、硫酸钾和硝酸钡反应生成白色沉淀硫酸钡和硝酸钾,取样,滴加Ba(NO3)2溶液,观察现象可以鉴别硝酸钾和硫酸钾;
B、碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,通过加入适量的CaCl2溶液,反应后过滤可以除去碳酸钠,但是带入新的杂质氯化钠,该选项设计不合理;
C、高温条件下,碳酸钙分解生成氧化钙和二氧化碳,通过高温加热到固体质量不变可以除去碳酸钙;
D、氢氧化钠溶于水放热,硝酸铵溶于水吸热,通过分别加入水中溶解,用手触摸烧杯外壁可以区分氢氧化钠和硝酸铵.
故选:B.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
12.下面是李好同学用连线的方式对某一主题知识进行归纳的情况,其中有错误的一组是( )
| A.性质与用途 氢气燃烧产物为水--最理想燃料 熟石灰呈碱性--改良酸性土壤 活性炭有吸附性--做净水剂 | B.元素与人体健康 人体缺氟--易生龋牙 人体缺锌--影响人体发育 人体缺碘--甲状腺肿大 |
| C.生活常识 取暖防中毒--煤炉上放一壶水 菜刀防生锈--喷水后悬挂起来 海鲜品保鲜--甲醛水溶液浸泡 | D.环保与物质的利用 减少水污染--合理使用农药、化肥 减少汽车尾气污染--使用乙醇汽油 减少白色污染--使用可降解的塑料 |
| A. | A | B. | B | C. | C | D. | D |
5.地球是一颗美丽的蓝色星球,海水占了全球水资源的97%.海水资源的开发和利用具有非常广阔的前景.
(1)海水中含有大量的NaCl,可用于制备钠及其化合物,其流程如图:

①加入过量Na2CO3溶液目的是除去CaCl2和BaCl2,流程中不能用过量稀硫酸代替过量稀盐酸的原因是会生成新的杂质硫酸钠;
②提纯过程中使用了过滤和蒸发操作,实验室过滤和蒸发操作均使用到的玻璃仪器是玻璃棒;
③流程图中制备金属钠的化学方程式为2NaCl$\frac{\underline{\;通电\;}}{\;}$2Na+Cl2↑.
(2)工业上利用电解饱和食盐水的方法制备NaOH,并同时获得两种单质.补充并配平化学方程式:
□NaCl+□H2O□NaOH+□H2↑+□Cl2↑
(3)刘廷在实验室找到一瓶长期放置的NaOH溶液,欲对其成分进行实验探究.
【查阅资料】
I.NaOH与CO2分两步反应:
2NaOH+CO2═Na2CO3+H2O;Na2CO3+CO2+H2O═2NaHCO3
Ⅱ.NaOH与NaHCO3反应方程式为:NaOH+NaHCO3═Na2CO3+H2O
Ⅲ.物质的溶解性:
溶液的酸碱性:BaCl2溶液呈中性
【提出猜想】刘廷根据资料中的I、Ⅱ对其成分提出了5种合理猜想,请将猜想补充完整
猜想1:只有NaOH,猜想2:含有氢氧化钠、碳酸钠,猜想3:只有Na2CO3,猜想4:碳酸氢钠、碳酸钠,
猜想5:只有NaHCO3.
【实验验证】
【实验结论】通过以上实验操作得出结论:猜想3是正确的(填数字)
(1)海水中含有大量的NaCl,可用于制备钠及其化合物,其流程如图:

①加入过量Na2CO3溶液目的是除去CaCl2和BaCl2,流程中不能用过量稀硫酸代替过量稀盐酸的原因是会生成新的杂质硫酸钠;
②提纯过程中使用了过滤和蒸发操作,实验室过滤和蒸发操作均使用到的玻璃仪器是玻璃棒;
③流程图中制备金属钠的化学方程式为2NaCl$\frac{\underline{\;通电\;}}{\;}$2Na+Cl2↑.
(2)工业上利用电解饱和食盐水的方法制备NaOH,并同时获得两种单质.补充并配平化学方程式:
□NaCl+□H2O□NaOH+□H2↑+□Cl2↑
(3)刘廷在实验室找到一瓶长期放置的NaOH溶液,欲对其成分进行实验探究.
【查阅资料】
I.NaOH与CO2分两步反应:
2NaOH+CO2═Na2CO3+H2O;Na2CO3+CO2+H2O═2NaHCO3
Ⅱ.NaOH与NaHCO3反应方程式为:NaOH+NaHCO3═Na2CO3+H2O
Ⅲ.物质的溶解性:
| CO32- | HCO3- | OH- | |
| Ba2+ | 不溶 | 溶 | 溶 |
【提出猜想】刘廷根据资料中的I、Ⅱ对其成分提出了5种合理猜想,请将猜想补充完整
猜想1:只有NaOH,猜想2:含有氢氧化钠、碳酸钠,猜想3:只有Na2CO3,猜想4:碳酸氢钠、碳酸钠,
猜想5:只有NaHCO3.
【实验验证】
| 步骤 | 操作 | 现象 | 结论 |
| 步骤1 | 取该NaOH溶液,加入过量BaCl2溶液 | 产生白色沉淀 | 证明猜想1、5不成立(填数字) |
| 步骤2 | 取步骤1中上层清液,滴加稀盐酸 | 无气泡产生 | 证明原溶液不含HCO3-、CO32-(填“离子”) |
| 步骤3 | 另取步骤1中上层清液,滴加酚酞 | 溶液未变红 | 证明原溶液不含OH-(填“离子”) |
12.下列物质的名称(或俗称)、化学式和类别,三者都正确的是( )
| A. | 烧碱、Na2CO3、碱 | B. | 消石灰、CaCO3、盐 | ||
| C. | 生石灰、CaO、氧化物 | D. | 碳酸氢铵、NH4HCO3、酸 |
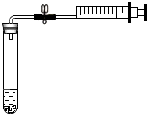 为测定空气中氧气的含量,小明同学设计如下方案:选用容积为40mL的试管作反应器,将白磷放入试管,用橡皮塞塞紧试管口,通过导管与容积为60mL针筒注射器组成如图的实验装置.假设此实验能按照小明的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:
为测定空气中氧气的含量,小明同学设计如下方案:选用容积为40mL的试管作反应器,将白磷放入试管,用橡皮塞塞紧试管口,通过导管与容积为60mL针筒注射器组成如图的实验装置.假设此实验能按照小明的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题: