题目内容
18.如图是氧化沉淀法生产复印用的高档Fe3O4粉的工艺流程简图,根据要求回答问题.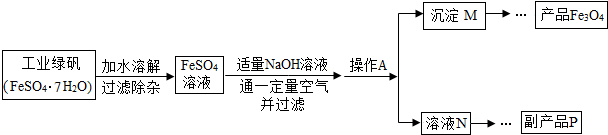
(1)铁的另两种常见氧化物的化学式是Fe2O3、FeO.
(2)加水溶解过程中,在实验室里通常要使用的玻璃仪器有烧杯和玻璃棒,操作A的名称是过滤.
(3)副产品P是硫酸钠,由溶液N获得该副产品的操作顺序是b→c→a→d.
a.过滤 b.加热浓缩 c.冷却结晶 d.晶体加热至完全失去结晶水
(4)通空气时的化学方程式是4Fe(OH)2+2H2O+O2$\frac{\underline{\;\;△\;\;}}{\;}$ 4Fe(OH)3,由沉淀M获得Fe3O4的过程中发生的反应为Fe(OH)2+2Fe(OH)3═Fe3O4+4H2O,控制“一定量空气”的目的是防止氢氧化亚铁全部被氧化为氢氧化铁,沉淀M中Fe(OH)2和Fe(OH)3的最佳质量比为45:107.(相对分子质量:Fe(OH)2:90;Fe(OH)3:107)
分析 (1)根据常见的铁的氧化物来分析;
(2)根据溶解的过程想用的仪器;
(3)根据氢氧化钠与硫酸亚铁反应的生成物来判断副产品,根据冷却热饱和溶液的过程考虑操作顺序;
(4)如果氧气过多会把氢氧化亚铁全部氧化,就得不到四氧化三铁了,根据方程式计算出Fe(OH)2和Fe(OH)3的相对分子质量比,别忘了前面的系数.
解答 解:(1)常见的铁的氧化物还有氧化铁和氧化亚铁,在氧化铁中,铁显+3价,氧化亚铁中铁显+2价,氧元素均为-2价,故填:Fe2O3;FeO;
(2)溶解时烧杯中盛放的是溶液,用玻璃棒搅拌即可,所以还需玻璃棒;在分离固体和液体混合物时用到的操作是过滤,所以操作A为过滤;
(3)氢氧化钠与硫酸亚铁反应的生成物是氢氧化亚铁与硫酸钠,因为氢氧化亚铁属于另一反应的反应物了所以副产品是硫酸钠;冷却热饱和溶液 的过程是先加热,再降温,析出晶体后过滤再通过加热除去结晶水即可;
(4)通过反应Fe(OH)2+2Fe(OH)3?Fe3O4+4H2O可知Fe(OH)2和Fe(OH)3都是反应物,如果不控制“一定量空气”氧气过多会把氢氧化亚铁全部氧化,就得不到四氧化三铁了;由化学方程式Fe(OH)2+2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2O可知Fe(OH)2和Fe(OH)3的最佳质量比为$\frac{90}{2×107}$=$\frac{45}{107}$.
故答案为:(1)Fe2O3;FeO;(2)玻璃棒;过滤;(3)硫酸钠;c;a;(4)防止氢氧化亚铁全部被氧化为氢氧化铁;45:107.
点评 通过回答本题知道了制取四氧化三铁的方法,溶解需要的仪器,由溶液析出晶体的方法.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案
相关题目
6.用“分子的观点”解释下列现象,错误的是( )
| A. | 轮胎充气--分子间有间隔 | B. | 湿衣晾干--分子不停地运动 | ||
| C. | 水结成冰--分子本身发生变化 | D. | 气体受热膨胀--分子间间隔变大 |
3.甲烷(CH4)气体难溶于水,不与浓硫酸、硫酸铜、碱石灰(氢氧化钠和氧化钙的固体混合物)、澄清石灰水等起反应.甲烷具有还原性,在加热条件下与氧化铜发生反应,生成铜、水和二氧化碳.
某化学小组为验证甲烷的组成,设计了如图所示实验.该实验装置气密性良好,实验中所用试剂均足量.
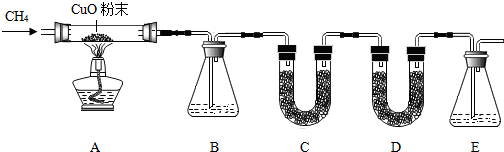
已知装置B、C、D、E中分别盛有浓硫酸、白色无水CuSO4固体、碱石灰、澄清石灰水,而且已知白色无水CuSO4固体遇水会变蓝色.
(1)实验步骤:
I.通入甲烷气体.
II.点燃酒精灯加热,反应一段时间后,停止加热.
III.继续通甲烷至玻璃管冷却.
(2)有关现象:
①A中黑色固体变红色;②中C中未见变蓝色;③E中未见出现浑浊.
(3)有关数据:
请回答下列问题:
(1)实验室若用无水醋酸钠固体和碱石灰混合加热制取甲烷,则发生装置类型与C相同.
A.用石灰石与稀盐酸制二氧化碳B.用过氧化氢制氧气C.用高锰酸钾制氧气
(2)甲烷还原氧化铜的化学方程式为CH4+4CuO$\frac{\underline{\;\;△\;\;}}{\;}$4Cu+2H2O+CO2.
(3)实验过程中通入甲烷的作用各不相同.步骤I是排尽除去装置中的空气;步骤II是还原氧化铜;步骤III是将生成的气体全部排出,减小实验误差.
(4)请根据该实验数据列计算式,证明甲烷中不含氧元素.相关计算式为108.0g-106.4g=(212.9g-212.0g)×$\frac{16}{18}$×100%+(131.1g-131.0g)×$\frac{32}{44}$×100%=1.6g.
某化学小组为验证甲烷的组成,设计了如图所示实验.该实验装置气密性良好,实验中所用试剂均足量.

已知装置B、C、D、E中分别盛有浓硫酸、白色无水CuSO4固体、碱石灰、澄清石灰水,而且已知白色无水CuSO4固体遇水会变蓝色.
(1)实验步骤:
I.通入甲烷气体.
II.点燃酒精灯加热,反应一段时间后,停止加热.
III.继续通甲烷至玻璃管冷却.
(2)有关现象:
①A中黑色固体变红色;②中C中未见变蓝色;③E中未见出现浑浊.
(3)有关数据:
| A中玻璃管及物质总质量/g | B装置及物质总质量/g | D装置及物质总质量/g | |
| 反应前 | 108.0 | 212.0 | 131.0 |
| 反应后 | 106.4 | 212.9 | 132.1 |
(1)实验室若用无水醋酸钠固体和碱石灰混合加热制取甲烷,则发生装置类型与C相同.
A.用石灰石与稀盐酸制二氧化碳B.用过氧化氢制氧气C.用高锰酸钾制氧气
(2)甲烷还原氧化铜的化学方程式为CH4+4CuO$\frac{\underline{\;\;△\;\;}}{\;}$4Cu+2H2O+CO2.
(3)实验过程中通入甲烷的作用各不相同.步骤I是排尽除去装置中的空气;步骤II是还原氧化铜;步骤III是将生成的气体全部排出,减小实验误差.
(4)请根据该实验数据列计算式,证明甲烷中不含氧元素.相关计算式为108.0g-106.4g=(212.9g-212.0g)×$\frac{16}{18}$×100%+(131.1g-131.0g)×$\frac{32}{44}$×100%=1.6g.
7.铝箔常用在食品包装上,因为铝具有良好的( )
| A. | 延展性 | B. | 导电性 | C. | 抗腐蚀性 | D. | 导热性 |
8.氢氟酸(HF)对玻璃有腐蚀作用,可用在玻璃上雕刻各种精美图案,也可用在玻璃仪器上标注刻度文字.氢氟酸与玻璃发生的反应可以表示为:SiO2+4HF═X↑+2H2O,下列说法正确的是( )
| A. | 一定含有硅元素、氟元素 | B. | 可能含有氧元素 | ||
| C. | 可能含有氢元素 | D. | X是一种氧化物 |
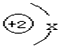 ,图中x为2,该原子的相对原子质量为3,原子核内中子数为1.
,图中x为2,该原子的相对原子质量为3,原子核内中子数为1.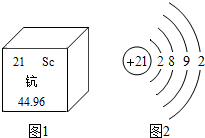 钪是稀土金属,主要用于航天合金材料.
钪是稀土金属,主要用于航天合金材料.