题目内容
13.请仔细阅读下列材料:材料一:l869年,俄国化学家门捷列夫对已发现的元素进行研究,制作了元素周期表(如表是其片断),并在他的元素周期表中留下了许多空位代表尚未发现的新元素,其中就预言了“类铝”这种新元素.
| 13 Al 铝 26.98 | 14 Si 硅 28.09 |
| 类铝 | 类硅 |
材料三:l876年,布瓦博德朗将金属镓提纯后测得镓的密度为5.94g•cm-3,从而验证了元素周期表的正确性.随后科学家根据元素周期表的空位,按图索骥,发现了许多新元素.目前金属镓广泛用于制造半导体材料.镓的原子结构示意图如图
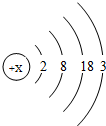 ,常见化合价为+3.
,常见化合价为+3.根据你的理解回答下列问题:
(1)镓元素原子的质子数为31,其原子最外层电子数为3;
(2)请根据上述材料,总结金属镓的有关知识:
物理性质:银白色金属,密度为5.94g•cm-3;
化学性质(请用化学方程式表示):2Ga+6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Ga(OH)3+3H2↑;
用途:制造半导体材料;
(3)氢氧化镓与氢氧化钠都具有碱的性质,则氢氧化镓与稀硫酸反应生成盐的化学式为_Ga2(SO4)3.
分析 (1)根据在原子中,质子数=核外电子数,进行解答;离原子核最远的是最外层,依据原子结构示意图即可解答;
(2)物质的色、味、态、熔、沸点、密度、硬度、水溶性等属于物理性质;物质的化学性质包括可燃性、氧化性、还原性、稳定性、酸性、碱性、热解性等,通常描述的语句中有能、可以、可等字眼儿进行解答;
(3)由于镓常见化合价为+3,硫酸根的根价为-2,利用十字交叉法即可写出化学式.
解答 解:(1)根据在原子中,质子数=核外电子数,由原子结构示意图可知镓元素原子的质子数为:31;
最外层电子数为:3;
(2)根据物质的色、味、态、熔、沸点、密度、硬度、水溶性等属于物理性质,从题中可知
镓的物理性质为:镓是银白色金属,密度为5.94g•cm-3;
根据镓能与沸水剧烈反应生成氢气和氢氧化镓反应化学方程式为:2Ga+6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Ga(OH)3+3H2↑;
根据目前金属镓广泛用于制造半导体材料,可知镓的用途为:制造半导体材料;
故答案为:银白色金属,密度为5.94g•cm-3; 2Ga+6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Ga(OH)3+3H2↑; 制造半导体材料;
(3)由于镓常见化合价为+3,硫酸根的根价为-2,利用十字交叉法写出硫酸镓的化学式为:Ga2(SO4)3;
故答案为:Ga2(SO4)3 .
答案:
(1)31 3
(2)银白色金属,密度为5.94g•cm-3;2Ga+6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Ga(OH)3+3H2↑; 制造半导体材料
(3)Ga2(SO4)3
点评 本题考查学生根据题中所给的信息及所学知识进行分析解题的能力,注意书写化学方程式的写配标等.

| A. | 用pH试纸不能区分肥皂水和食醋 | |
| B. | 用灼烧的方法能区别棉花和羊毛 | |
| C. | 发生复分解反应产物中有水或气体或沉淀产生 | |
| D. | 用饱和(NH4)2SO4溶液能区分食盐水和蛋白质溶液 |
| A. | H2SO4 NaNO3 KOH | B. | FeCl3 BaCl2 Mg(NO3)2 | ||
| C. | Na2SO4 KCl NaCl | D. | KNO3 K2SO4 BaCl2 |
| A. | 往水中扔垃圾 | B. | 在水中洗衣服 | C. | 在水中乘船 | D. | 在水中游泳 |

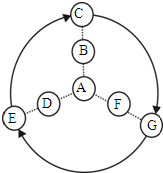 如图表示初中常见几种不同化合物之间的关系,图中虚线两端的化合物可以转化或相互反应,箭头表示物质间存在转化关系;反应条件、部分反应物和生成物已略去.请根据以下每小题的具体情况进行解答.
如图表示初中常见几种不同化合物之间的关系,图中虚线两端的化合物可以转化或相互反应,箭头表示物质间存在转化关系;反应条件、部分反应物和生成物已略去.请根据以下每小题的具体情况进行解答.