题目内容
19.化学就在我们身边,它与我们的生活息息相关.(1)请从“氧气、稀有气体、二氧化碳、水蒸气”中选择适当的物质填空
①露在空气中的饼干变软是因为空气中有水蒸气
②可用于电光源的气体是稀有气体
③可用于炼钢、气焊的气体是氧气
④能使澄清石灰水变浑浊的气体是二氧化碳
(2)通过“对人体吸入空气和呼出气体的探究”,我们可以知道呼出气体与吸入空气相比,含量增多的成分是水蒸气、二氧化碳,呼出气体中含量最多的成分是氮气
(3)写出下列具体粒子的名称:二氧化碳由二氧化碳分子构成,铁由铁原子构成.
分析 (1)根据空气的成分及其性质用途来分析;
(2)人呼吸时把空气中的氧气转化为二氧化碳,同时从体内带出水蒸汽,人体呼出气体和空气中的氧气、二氧化碳、水蒸汽含量不同,呼出的气体与吸入空气相比,具有“两多一少”的特点,即与吸入的空气相比,二氧化碳、水蒸气含量增加,氧气含量减少,据此分析解答即可;
(3)根据构成物质的粒子来分析.
解答 解:(1)①露在空气中的饼干变软是因为空气中有水蒸气,故填:水蒸气;
②稀有气体在通电时能发出有色的光,可用作制造电光源,故填:稀有气体;
③氧气具有助燃性,常用于炼钢、气焊;故填:氧气;
④二氧化碳与氢氧化钙反应生成了碳酸钙沉淀和水,所以能使澄清石灰水变浑浊,故填:二氧化碳;
(2)呼出气体与吸入空气相比,含量增多的成分是水蒸气、二氧化碳,呼出气体中含量最多的成分是氮气;故填:水蒸气、二氧化碳,氮气;
(3)二氧化碳是由二氧化碳分子构成的,铁是由铁原子构成的,故填:二氧化碳分子,铁原子.
点评 本题难度不大,了解空气的组成、呼吸作用的原理、人体吸入的空气与呼出的气体成分的区别是正确解答本题的关键.

练习册系列答案
相关题目
11.为了测定某石灰石中碳酸钙的质量分数.取石灰石样品,与足量质量分数为7.3%的稀盐酸在烧杯(烧杯质量为20g)中充分反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水).有关实验数据如下表:
(1)配制上述质量分数为7.3%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是20g;
(2)发生反应的化学方程式为CaC03+2HCl=CaCl2+H20+C02↑;
(3)求解llg该石灰石样品中碳酸钙质量(x)的比例式为$\frac{100}{x}=\frac{44}{4.4g}$;
(4)向反应后所得溶液中加入5.4g水后,则最终溶液中溶质的质量分数是10%;
(5)该水泥厂用该石灰石制得生石灰56t,理论上需要该石灰石的质量是66t.
| 反应前 | 反应后 | ||
| 实验 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和混合物的质量 |
| 数据 | 120g | 11g | 126.6g |
(2)发生反应的化学方程式为CaC03+2HCl=CaCl2+H20+C02↑;
(3)求解llg该石灰石样品中碳酸钙质量(x)的比例式为$\frac{100}{x}=\frac{44}{4.4g}$;
(4)向反应后所得溶液中加入5.4g水后,则最终溶液中溶质的质量分数是10%;
(5)该水泥厂用该石灰石制得生石灰56t,理论上需要该石灰石的质量是66t.
14.下列变化中,属于化学变化的是( )
| A. | 海水晒盐 | B. | 蜡烛熔化 | C. | 食物霉变 | D. | 汽油挥发 |
9.实验室制取氧气不选用的是( )
| A. | 高锰酸钾 | B. | 氯酸钾 | C. | 空气 | D. | 过氧化氢 |
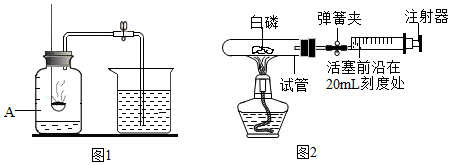
 研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置.请根据图示实验回答下列问题.
研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置.请根据图示实验回答下列问题.