题目内容
2.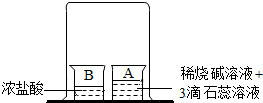 根据“如图”实验,判断下列说法错误的是( )
根据“如图”实验,判断下列说法错误的是( )| A. | 浓盐酸有挥发性 | B. | HCl分子在运动 | ||
| C. | A杯溶液的颜色会改变 | D. | A杯内发生了置换反应 |
分析 浓盐酸具有挥发性,挥发出来的氯化氢气体,溶于水形成盐酸,酸能使紫色的石蕊试液变红色.
解答 解:A.浓盐酸具有挥发性,故正确;
B.此现象也说明了氯化氢分子在不断的运动,故正确;
C.挥发出来的氯化氢气体,溶于水形成盐酸,酸和碱反应,A杯溶液的颜色会改变,故正确;
D.盐酸和氢氧化钠反应属于复分解反应,不是置换反应,故错误.
故选D.
点评 本题考查了分子的基本性质,完成此题,可以依据已有的分子的性质和题中信息进行.

练习册系列答案
相关题目
12.某学校化学兴趣小组的同学们在实验室发现一瓶石灰水试剂瓶瓶壁和瓶塞周围有一些白色粉末.为了弄清楚白色粉末的成分及形成原因,他们进行了如下探究:
【提出问题】白色粉末成分的猜想和成因分析.
【做出猜想】①可能是CaCO3,原因是石灰水与空气中的CO2反应.
②可能是Ca(OH)2 ,原因是溶剂蒸发,石灰水中的溶质结晶析出.
③还可能是以上二者的混合物.
【实验探究】甲同学取白色粉末于试管中,加少量的水、震荡,发现试管底部有白色固体,于是他得出白色粉末是CaCO3的结论.乙同学认为甲同学的结论不严密,理由是Ca(OH)2微溶于水.
为了得出较严密的结论,他们进行了下表所示实验,请完成实验报告:
由上述实验可知,白色粉末成分的猜想③是正确的.
【拓展反思】
通过上述实验的探究,同学们向实验员提出了保存、使用易变质溶液的下列建议,合理的是ab.
a.密封保存 b.使用前临时配制 c.禁止使用该试剂.
【提出问题】白色粉末成分的猜想和成因分析.
【做出猜想】①可能是CaCO3,原因是石灰水与空气中的CO2反应.
②可能是Ca(OH)2 ,原因是溶剂蒸发,石灰水中的溶质结晶析出.
③还可能是以上二者的混合物.
【实验探究】甲同学取白色粉末于试管中,加少量的水、震荡,发现试管底部有白色固体,于是他得出白色粉末是CaCO3的结论.乙同学认为甲同学的结论不严密,理由是Ca(OH)2微溶于水.
为了得出较严密的结论,他们进行了下表所示实验,请完成实验报告:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取上述试管中的上层清液,滴加1~2滴酚酞试夜 | 溶液呈红色 | 白色粉末中有氢氧化钙 |
| ②往上述试管残留的白色固体中加入加入稀盐酸 | 有气泡产生 | 白色粉末中含有CaCO3 |
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【拓展反思】
通过上述实验的探究,同学们向实验员提出了保存、使用易变质溶液的下列建议,合理的是ab.
a.密封保存 b.使用前临时配制 c.禁止使用该试剂.
7.”国富民强”,我国制碱工业的先驱-侯德榜,在积贫积弱的旧中国与诺贝尔奖无缘.“侯氏制碱”制得的是( )
| A. | NaOH | B. | NaHCO3 | C. | Na2CO3 | D. | Ca(OH)2 |
18.五氧化二钒(V2O5)可用于冶炼钒钢,其中钒(V)元素的化合价是( )
| A. | +5 | B. | +3 | C. | +2 | D. | +1 |
19.以下对O2、CO2、SO2、MnO2四种物质组成的说法中,正确的是( )
| A. | 都含有氧分子 | B. | 都是氧化物 | C. | 都含有2个氧原子 | D. | 都含有氧元素 |
 电动自行车广泛使用大量材料,如图所示.
电动自行车广泛使用大量材料,如图所示.