题目内容
11.回答实验室制取氧气的相关问题.(1)写出高锰酸钾制取氧气的化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)如图1所示,高锰酸钾制取氧气发生装置应选用A(填编号,下同),以下气体收集装置不能采用的是E;
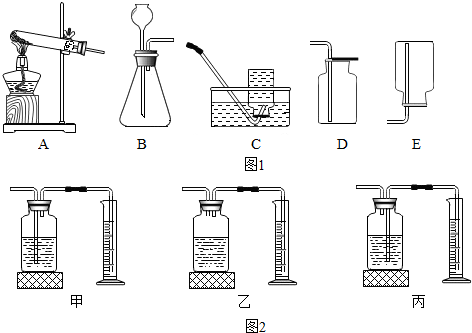
(3)为测定高锰酸钾分解生成氧气的体积,应选用图2中装置丙(填编号);
(4)若用B装置作为发生装置制取氧气则反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.为测定高锰酸钾分解生成氧气的体积,应选用图2中装置丙,丙装置氧气进入可以把水排出.
解答 解:(1)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)如果用高锰酸钾制氧气就需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;故答案为:A;E;
(3)为测定高锰酸钾分解生成氧气的体积,应选用图2中装置丙,丙装置氧气进入可以把水排出;故答案为:丙;
(4)过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平,故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的体积的测量等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
1.检验CO2常用的试剂是( )
| A. | 澄清的石灰水 | B. | 水 | C. | 盐酸 | D. | 石蕊试液 |
19.不需要其他试剂就可以将下列物质一一鉴别开来的是( )
| A. | K2CO3溶液、CaCl2溶液、KNO3溶液、稀盐酸 | |
| B. | KCl溶液、FeCl3溶液 Mg(NO3)2溶液 NaOH溶液 | |
| C. | Na2CO3溶液 KCl溶液 AgNO3溶液 NaOH溶液 | |
| D. | 稀硫酸、NaOH溶液 CuSO4溶液稀盐酸 |
6.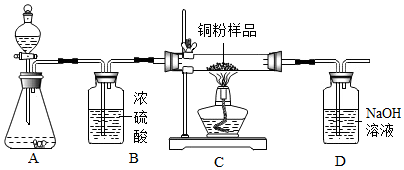 某化学兴趣小组用过氧化氢溶液(MnO2作催化剂)制取干燥的氧气,并用来测定10g某铜粉样品(含杂质碳)中铜的质量分数,实验装置如图所示.
某化学兴趣小组用过氧化氢溶液(MnO2作催化剂)制取干燥的氧气,并用来测定10g某铜粉样品(含杂质碳)中铜的质量分数,实验装置如图所示.
(1)装置B中浓硫酸的作用是吸收水蒸气.
(2)装置D中发生反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.小刚同学认为通过称量反应前后装置D的质量,进行计算便可求出样品中铜的质量分数.小婷同学认为小刚的方法有缺陷,原因是空气中含有的二氧化碳会进入D中被氢氧化钠溶液吸收,通过讨论,认为如果要用小刚同学的方法准确求出铜的质量分数,则应该在装置D之后连接一个装有碱石灰的干燥管消除影响.
(3)实验完毕,小聪同学误将用剩的H2O2溶液和装置C中的剩余固体仪器倒入烧杯中,发现有大量的气泡产生,经检验确认产生的气体是氧气.小明和小红两位同学对此颇感兴趣,进而展开了他们的探究之旅.
【提出问题】是粉末中的哪种物质加快了H2O2的分解速率?
【大胆猜想】猜想Ⅰ:剩余固体中的氧化剂加快了H2O2的分解速率;
猜想Ⅱ:剩余固体中的铜粉加快了H2O2的分解速率;
【实验设计】
【烦死拓展】同学们讨论后认为,上述实验还不能够确切地说明氧化铜就是过氧化氢分解制取氧气的催化剂,理由是不能确定反应前后氧化铜的质量和化学性质是否改变.
 某化学兴趣小组用过氧化氢溶液(MnO2作催化剂)制取干燥的氧气,并用来测定10g某铜粉样品(含杂质碳)中铜的质量分数,实验装置如图所示.
某化学兴趣小组用过氧化氢溶液(MnO2作催化剂)制取干燥的氧气,并用来测定10g某铜粉样品(含杂质碳)中铜的质量分数,实验装置如图所示.(1)装置B中浓硫酸的作用是吸收水蒸气.
(2)装置D中发生反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.小刚同学认为通过称量反应前后装置D的质量,进行计算便可求出样品中铜的质量分数.小婷同学认为小刚的方法有缺陷,原因是空气中含有的二氧化碳会进入D中被氢氧化钠溶液吸收,通过讨论,认为如果要用小刚同学的方法准确求出铜的质量分数,则应该在装置D之后连接一个装有碱石灰的干燥管消除影响.
(3)实验完毕,小聪同学误将用剩的H2O2溶液和装置C中的剩余固体仪器倒入烧杯中,发现有大量的气泡产生,经检验确认产生的气体是氧气.小明和小红两位同学对此颇感兴趣,进而展开了他们的探究之旅.
【提出问题】是粉末中的哪种物质加快了H2O2的分解速率?
【大胆猜想】猜想Ⅰ:剩余固体中的氧化剂加快了H2O2的分解速率;
猜想Ⅱ:剩余固体中的铜粉加快了H2O2的分解速率;
【实验设计】
| 实验操作 | 实验现象 | 分析及结论 |
| 实验一:将带火星的木条伸入盛有5mL5%H2O2溶液的试管 | 带火星的木条不能复燃 | H2O2溶液常温下产生氧气的量很少,不足以使带火星的木条复燃 |
| 实验二:向盛有5mL5%H2O2溶液的试管中加入1g氧化铜固体,将一根带火星的木条伸入试管 | 产生大量气泡,带火星的木条复燃 | 氧化铜能够加快过氧化氢的分解速率 |
| 实验三: 向盛有5mL5%H2O2溶液的试管中加入1g铜粉,将一根带火星的木条伸入试管 | 带火星的木条不能复燃 | 猜想Ⅱ不成立 |