题目内容
2.低钠盐适合患有高血压、心脏病的患者服用,苹果酸钠盐(C4H5O5Na)是低钠盐的一种.请回答:(1)苹果酸钠盐由四种元素组成,其中碳、氢、氧、钠的原子个数比是4:5:5:1.
(2)苹果酸钠盐的相对分子质量是156.其中各元素的质量比为C:H:O:Na=48:5:80:23.
(3)某病人每天使用3.12g苹果酸钠盐,其实摄入钠元素0.46克.
分析 (1)根据苹果酸钠化学式的含义进行分析判断,根据苹果酸钠的微观构成进行分析判断;
(2)根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行分析解答.根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行分析解答;
(3)利用元素的质量等于物质的质量与该元素的质量分数的乘积进行分析解答.
解答 解:(1)苹果酸钠是由碳、氢、氧、钠四种元素组成的,1个苹果酸钠分子是由4个碳原子、5个氢原子、5个氧原子和1个钠原子构成的,故填:四;4:5:5:1;
(2)根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得苹果酸钠盐的相对分子质量为:12×4+5+16×5+23=156.
根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得苹果酸钠盐中各元素的质量比为(12×4):(1×5):(16×5):23=48:5:80:23.
故填:156;48:5:80:23;
(3)3.12g苹果酸钠盐中的钠元素质量为3.12g×$\frac{23}{156}×100%$=0.46g;故填:0.46.
点评 本题难度不大,考查学生对相对分子量及化合物中各元素质量比的理解与掌握,利用物质中某元素的质量分数进行分析解题的能力.

练习册系列答案
相关题目
12.下列关于原子、离子结构叙述中,正确的是( )
| A. | 原子核都是由质子和中子构成的 | |
| B. | 最外层电子决定原子种类 | |
| C. | 原子的最外层电子数不超过8 | |
| D. | 最外层电子数为8的粒子一定是稀有气体原子 |
14.下列情况:①汽车排放的尾气;②水蒸发的水蒸汽;③化工厂排放的废气;④植物光合作用放出的气体;⑤煤燃烧产生的烟尘.其中,会使空气受到污染的是( )
| A. | ①②③⑤ | B. | ①③④ | C. | ②④⑤ | D. | ①③⑤ |
11.配平下列化学方程式
①8NH3+6NO2=7N2+12H2O;
②16P+15H2O=10PH3+3P2O5;
③1C2H6O+3O2=2CO2+3H2O;
④1CH4+2O2=1CO2+2H2O.
①8NH3+6NO2=7N2+12H2O;
②16P+15H2O=10PH3+3P2O5;
③1C2H6O+3O2=2CO2+3H2O;
④1CH4+2O2=1CO2+2H2O.
12.做完“铁在氧气里燃烧”实验后,小明同学有两个疑惑不解的问题,于是他进行了以下探究活动,请你一同参与.
【问题1】铁燃烧时溅落下来的黑色物质中还有没有铁呢?
【查阅资料1】
(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
(2)铁的氧化物均能溶于酸的溶液,但不产生氢气.
(3)颜色:Fe粉-黑色,FeO-黑色,Fe3O4-黑色,Fe2O3-红棕色
【实验探究】
将冷却后的黑色物质碾碎,装入试管,加入稀盐酸溶液,观察到的现象是产生气泡,说明铁燃烧时溅落下来的黑色物质中还含有铁.
【问题2】铁燃烧的产物为什么不是Fe2O3呢?
【查阅资料2】
(1)Fe3O4和Fe2O3的分解温度、铁的熔点见表:
(2)Fe2O3高温时分解成Fe3O4.
【理论探讨】
根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在1400℃~1538℃之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产生是Fe3O4.
【拓展延伸】
(1)实验中为了防止集气瓶炸裂,必须在集气瓶底部铺一层细沙,或加入适量的水;
(2)Fe2O3高温时会分解成Fe3O4和一种气体,请写出此反应的化学方程式6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑;
(3)有些超市的食品密封包装盒的透明盖内放有FeO粉末,若粉末的颜色由黑色变成红棕色,就说明包装盒破损进气,这样售货员就能及时发现并处理.
【问题1】铁燃烧时溅落下来的黑色物质中还有没有铁呢?
【查阅资料1】
(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
(2)铁的氧化物均能溶于酸的溶液,但不产生氢气.
(3)颜色:Fe粉-黑色,FeO-黑色,Fe3O4-黑色,Fe2O3-红棕色
【实验探究】
将冷却后的黑色物质碾碎,装入试管,加入稀盐酸溶液,观察到的现象是产生气泡,说明铁燃烧时溅落下来的黑色物质中还含有铁.
【问题2】铁燃烧的产物为什么不是Fe2O3呢?
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
(1)Fe3O4和Fe2O3的分解温度、铁的熔点见表:
(2)Fe2O3高温时分解成Fe3O4.
【理论探讨】
根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在1400℃~1538℃之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产生是Fe3O4.
【拓展延伸】
(1)实验中为了防止集气瓶炸裂,必须在集气瓶底部铺一层细沙,或加入适量的水;
(2)Fe2O3高温时会分解成Fe3O4和一种气体,请写出此反应的化学方程式6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑;
(3)有些超市的食品密封包装盒的透明盖内放有FeO粉末,若粉末的颜色由黑色变成红棕色,就说明包装盒破损进气,这样售货员就能及时发现并处理.
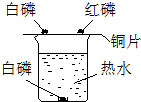 探究燃烧条件的实验装置如图所示.
探究燃烧条件的实验装置如图所示.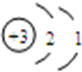 ,则锂离子的符号为Li+.
,则锂离子的符号为Li+.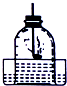 如图是某同学测定空气中氧气含量的实验装置.玻璃钟罩事先放入水槽中,并将水面以上的空气分成五等分,燃烧匙中放有过量红磷,在空气中点燃后迅速插入玻璃钟罩中并塞紧,请根据实验回答问题:
如图是某同学测定空气中氧气含量的实验装置.玻璃钟罩事先放入水槽中,并将水面以上的空气分成五等分,燃烧匙中放有过量红磷,在空气中点燃后迅速插入玻璃钟罩中并塞紧,请根据实验回答问题: