题目内容
4.某学习小组测定石灰石样品中碳酸钙的质量分数,取石灰石样品(样品中的杂质不溶于水,也不参与反应)25g,将100g稀盐酸分五次加入,实验过程所得数据如下表.请计算:| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 剩余固体质量/g | 20 | 15 | 10 | 7 | n |
(2)盐酸中溶质的质量分数.(结果精确到0.1%)
分析 (1)根据第一、二、三次加入盐酸后,固体质量都减少5g,第四次加入盐酸后,固体减少3g,所以n的值是7,所以参加反应的碳酸钙的质量就是18g,然后计算碳酸钙的质量分数;
(2)根据化学方程式和参加反应的盐酸的质量进行计算.
解答 解:(1)第一、二、三次加入盐酸后,固体质量都减少5g,第四次加入盐酸后,固体减少3g,所以n的值是7,所以参加反应的碳酸钙的质量就是18g,所以样品中碳酸钙的质量分数为:$\frac{25g-7g}{25g}$×100%=72%;
(2)设20g稀盐酸中氯化氢的质量为x
CaCO3+2HCl=CaCl2+H20+CO2↑
100 73
5g x
$\frac{100}{5g}$=$\frac{73}{x}$
x=3.65g
所以盐酸的溶质质量分数为:$\frac{3.65g}{20g}$×100%=18.3%.
故答案为:(1)72%;
(2)18.3%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
12.下列变化属于物理变化的是( )
| A. | 蜡烛燃烧 | B. | 农家肥腐熟 | C. | 汽油挥发 | D. | 粮食酿酒 |
19.下列对分子的认识,说法不正确的是( )
| A. | 墙内开花墙外香,说明分子在不停地运动 | |
| B. | “破镜不能重圆”,说明分子间有斥力 | |
| C. | 水与酒精混合后总体积变小,说明分子间有间隔 | |
| D. | 一氧化碳、二氧化碳的化学性质不同,是因为它们分子的构成不同 |
4.小明用托盘天平称取12.5克食盐时,发现指针向右偏转,则他应该( )
| A. | 移动游码 | B. | 添加食盐 | ||
| C. | 加法码 | D. | 调节天平的平衡螺母 |
2.3.3.3.2011 年 11 月 28 口,长春市有母子二人饮用了美汁源果粒奶优的饮料后,发生食物中毒,孩子死亡.近日长春还发生一起 2 人饮用该饮料后的中毒事件.经公安部门检验认定,这两起事件剩余饮料中均含有高毒性杀虫剂 ( 万灵 ) 的成分.万灵的化学式为 C5H10N2O2S,下列关于万灵的说法正确的是( )
| A. | 万灵是由五种元素组成的混合物 | |
| B. | 万灵中氮、氧元素质量比为 1:1 | |
| C. | 万灵由 5 个碳原子、10 个氢原子、2 个氮原子、2 个氧原子、1 个硫原子构成 | |
| D. | 万灵中碳元素的质量分数最大 |
 双燃料环保汽车在我市已投入使用,这种汽车所用的燃料是汽油或压缩天然气.
双燃料环保汽车在我市已投入使用,这种汽车所用的燃料是汽油或压缩天然气.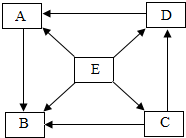 如图是一些物质的转化关系,“→”表示一种物质转化成另一种物质.其中A、B、C、D、E都含有同一种元素,且A、B、C、D属于同类别的化合物.A在生活中可用作调味品.C、D、E的水溶液能使酚酞溶液变红.部分反应物、生成物及反应条件已省略.
如图是一些物质的转化关系,“→”表示一种物质转化成另一种物质.其中A、B、C、D、E都含有同一种元素,且A、B、C、D属于同类别的化合物.A在生活中可用作调味品.C、D、E的水溶液能使酚酞溶液变红.部分反应物、生成物及反应条件已省略.