题目内容
13.A~E五种物质分别由H、O、C、Cl、Ca五种元素中的两种或三种组成,请回答下列问题.(1)A物质是生石灰的主要成分,A的化学式为CaO.
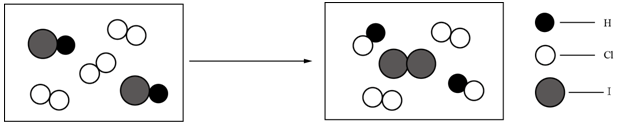
(2)B物质中两种元素的原子个数比为1:1,其分解时可以产生氧气,B为过氧化氢.
(3)向NaOH溶液依次加入C、D溶液、E溶液和紫色石蕊溶液,现象如图所示.

①C和D两种物质分别是CO2和Ca(OH)2.
②加入E后沉淀溶解并产生大量气泡,用化学方程式表示产生此现象的原因CaCO3+2HCl=CaCl2+H2O+CO2↑.
③红色溶液中含有的物质有水、石蕊、HCl、CaCl2、NaCl.
分析 根据物质的性质进行分析解答,生石灰是氧化钙的俗称;过氧化氢中氢原子和氧原子的个数比为1:1,能分解生成氧气,同时生成水;氢氧化钠溶液中加入C,得到无色溶液,加入D物质,能生成白色沉淀,白色沉淀加入E,能产生气泡,说明产生的沉淀是碳酸盐,最后加入石蕊试液,溶液变红,说明E是酸,故D可能是碳酸钠,氢氧化钠能与二氧化碳反应生成碳酸钠,故C是二氧化碳,据此解答.
解答 解:生石灰是氧化钙的俗称;过氧化氢中氢原子和氧原子的个数比为1:1,能分解生成氧气,同时生成水;氢氧化钠溶液中加入C,得到无色溶液,加入D物质,能生成白色沉淀,白色沉淀加入E,能产生气泡,说明产生的沉淀是碳酸盐,最后加入石蕊试液,溶液变红,说明E是酸,故D可能是碳酸钠,氢氧化钠能与二氧化碳反应生成碳酸钠,故C是二氧化碳,带入题干,推断合理;
①C是二氧化碳,D是氢氧化钙,故填:CO2和Ca(OH)2.
②加入E后沉淀溶解并产生大量气泡,是生成的碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,故填:CaCO3+2HCl=CaCl2+H2O+CO2↑.
③红色溶液中含有的物质有水、石蕊、盐酸、生成的氯化钙和氯化钠,故填:HCl、CaCl2、NaCl.
点评 本题考查的是常见的物质推断,完成此题,可以依据已有的物质的性质以及物质间反应的现象进行.

练习册系列答案
相关题目
3.下列化学用语表示正确的是( )
| A. | 氧化铁:FeO | |
| B. | 二个氢原子:2H | |
| C. | 正二价的镁元素:Mg+2 | |
| D. | 铝与盐酸的反应:Al+2HCl=AlCl2+H2↑ |
5.下列有关实验操作或实验现象正确的是( )
| A. | 红磷燃烧产生大量的白雾 | |
| B. | 铁丝伸入盛有氧气的集气瓶中剧烈燃烧 | |
| C. | 加热试管中的药品时,试管口要向下倾斜 | |
| D. | 硫在空气燃烧,产生淡蓝色火焰和刺激燃气味的气体 |
2.化学是以实验为基础的学科.下列有关实验现象的描述中,正确的是( )
| A. | 向氯化铜溶液中滴加氢氧化钠溶液,有白色沉淀生成 | |
| B. | 硫粉在氧气中燃烧产生蓝紫色火焰,生成有刺激性气味的气体 | |
| C. | 将铁丝插入硫酸铜溶液中,铁丝上会有红色固体生成,溶液变成黄色 | |
| D. | 电解水实验中,与电源正、负极相连的电极上产生的气体的体积比为1:8 |
3.包河区因包河而得名,因包公而闻名.素有“合肥文脉”之美誉.近几年发展迅猛,正着カ打造“安徽新中心.品质首善区“.以下与之有关事物或做法,发生化学変化的是( )
| A. |  制包河美酒 | B. |  推土修建適路 | C. |  规划滨湖蓝图 规划滨湖蓝图 | D. |  引水治巢湖污染 引水治巢湖污染 |