题目内容
2013年12月14日21时11分,嫦娥三号成功着陆于月球表面,开始对月球进行勘探,嫦娥三号的着陆器以液氢、液氧做推进剂.
(1)分离法获取氧气:分离液态空气法制氧气,是利用空气中各成分的 不同进行分离的;
(2)实验室获取氧气,加热高锰酸钾获取氧气的化学方程式是
(3)电解水法获取氢气:氢气在于电源 (填“正”或“负”)极相连的电极上产生,它与产生氧气的体积比为
(4)水煤气法获取氢气:用焦炭(主要成分是谈单质)为原料与水蒸汽在高温时反应制得H2和CO,反应的化学方程式为
(5)氢能源是理想的能源,但还不能广泛使用的原因是 .
(1)分离法获取氧气:分离液态空气法制氧气,是利用空气中各成分的
(2)实验室获取氧气,加热高锰酸钾获取氧气的化学方程式是
(3)电解水法获取氢气:氢气在于电源
(4)水煤气法获取氢气:用焦炭(主要成分是谈单质)为原料与水蒸汽在高温时反应制得H2和CO,反应的化学方程式为
(5)氢能源是理想的能源,但还不能广泛使用的原因是
考点:氧气的工业制法,实验室制取氧气的反应原理,电解水实验,书写化学方程式、文字表达式、电离方程式,氢气的用途和氢能的优缺点
专题:空气与水,氧气、氢气的性质与用途
分析:(1)根据分离液态空气法制氧气的原理和过程回答;
(2)根据高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气解答;
(3)电解水时,正极产生氧气,有助燃性;负极产生氢气,具有可燃性解答;
(4)根据信息:将煤(主要成分是碳)在高温条件下与水蒸气反应,制得水煤气(CO和H2的混合气体).写出化学反应式;
(5)根据氢能是理想的能源,还不能广泛使用的原因是制取成本高、储运困难解答;
(2)根据高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气解答;
(3)电解水时,正极产生氧气,有助燃性;负极产生氢气,具有可燃性解答;
(4)根据信息:将煤(主要成分是碳)在高温条件下与水蒸气反应,制得水煤气(CO和H2的混合气体).写出化学反应式;
(5)根据氢能是理想的能源,还不能广泛使用的原因是制取成本高、储运困难解答;
解答:解:
(1)分离液态空气法制氧气的过程是:先把空气加压、降温,使之变成液体,然后逐渐升温,沸点低的氮气先挥发出来,剩余部分主要就是氧气,可见是利用了空气中氮气和氧气的沸点不同;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;反应的化学方程式为:2KMnO4
K2MnO4+MnO2+O2↑;
(3)做水的电解实验时,与电源负极相连的电极上产生的气体是氢气,与电源正极相连的电极上产生的气体是氧气,其体积比约是2:1.
(4)根据信息:将煤(主要成分是碳)在高温条件下与水蒸气反应,制得水煤气(CO和H2的混合气体),可知化学反应式是:H2O+C
CO+H2.
(5)氢能是理想的能源,还不能广泛使用的原因是制取成本高、储运困难;
答案:
(1)沸点
(2)2KMnO4
K2MnO4+MnO2+O2↑;
(3)负 2:1
(4)H2O+C
CO+H2
(5)制取成本高、储运困难
(1)分离液态空气法制氧气的过程是:先把空气加压、降温,使之变成液体,然后逐渐升温,沸点低的氮气先挥发出来,剩余部分主要就是氧气,可见是利用了空气中氮气和氧气的沸点不同;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;反应的化学方程式为:2KMnO4
| ||
(3)做水的电解实验时,与电源负极相连的电极上产生的气体是氢气,与电源正极相连的电极上产生的气体是氧气,其体积比约是2:1.
(4)根据信息:将煤(主要成分是碳)在高温条件下与水蒸气反应,制得水煤气(CO和H2的混合气体),可知化学反应式是:H2O+C
| ||
(5)氢能是理想的能源,还不能广泛使用的原因是制取成本高、储运困难;
答案:
(1)沸点
(2)2KMnO4
| ||
(3)负 2:1
(4)H2O+C
| ||
(5)制取成本高、储运困难
点评:本题考查了有关氧气的工业制法和电解水以及氢能的使用的知识,完成此题,可以依据已有的知识进行.电解水实验的重要现象:与负极相连的试管产生氢气,与电源正极相连的试管产生的为氧气,两种气体体积比为2:1

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
江西素有“红土地”之称,其土壤偏酸性,下列作物不适宜在江西种植的是( )
| 作 物 | 茶树 | 柑桔 | 西瓜 | 甘草 |
| 最适宜种植的土壤pH范围 | 5.0-5.5 | 5.0-5.7 | 6.0-7.0 | 7.2-8.5 |
| A、茶树 | B、柑桔 | C、西瓜 | D、甘草 |
下列家庭用的物品中,与水充分混合后,不能形成溶液的是( )
| A、白醋 | B、面粉 | C、味精 | D、蔗糖 |
自然界中存在着碳、氧循环,维持着大气成分的相对稳定,创造和谐的生存环境.下列关于其说法不正确的是( )
| A、大气中的二氧化碳气体仅仅来源动植物的呼吸 |
| B、引发温室效应的气体主要是二氧化碳 |
| C、以二氧化碳为主要原料通过光合作用可以制取氧气 |
| D、燃料的燃烧和动植物的呼吸消耗氧气 |
下列关于氧气的说法,错误的是( )
| A、实验室制取氧气时,一定要加催化剂 |
| B、氧气的化学性质比氮气活泼 |
| C、油锅着火,可用锅盖盖灭,依据的灭火原理是隔绝氧气 |
| D、氧气能与大多数的金属、某些化合物反应,化学性质比较活泼 |
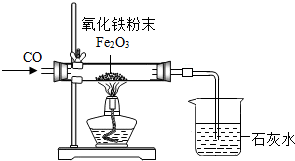 一无色气体,可能有H2,CO,CO2中的一种或数种,现将无色气体进行如图所示的实验,观察到甲装置中红色粉末变成黑色物质,烧杯中澄清的石灰水变浑浊,下列分析正确的是( )
一无色气体,可能有H2,CO,CO2中的一种或数种,现将无色气体进行如图所示的实验,观察到甲装置中红色粉末变成黑色物质,烧杯中澄清的石灰水变浑浊,下列分析正确的是( )| A、该气体中一定有还原性气体和CO2 |
| B、该气体中可能有碳的氧化物 |
| C、该气体一定是混合物 |
| D、该气体一定有还原性气体,一定有碳的氧化物 |
如图是小明同学在“化学实验操作考查”中相关的实验操作,其中正确的是( )
A、 熄灭酒精灯 |
B、 取用固体药品 |
C、 用橡胶塞塞住试管 |
D、 称取固体药品 |
