题目内容
8.根据如图原子或离子结构示意图回答问题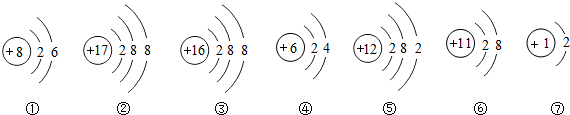
(1)最容易得到电子的原子是(填序号)①;表示阳离子有(填序号)⑥;微粒⑦的符号是H-;③与⑥形成化合物的化学式为Na2S;
(2)从上述结构示意图表示的元素中选择适当元素,按下列要求写出化学式(每空只写一个):
含有+6价元素的酸H2SO4,能与酸反应的氧化物Na2O,生活中重要的调味剂NaCl,含有三种元素的有机化合物C2H5OH.
分析 根据微粒的结构示意图的意义分析,当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子,根据最外层电子数分析元素的性质,根据常见元素组成的物质及性质写出有关的化学式.
解答 解:(1)在①中,核内质子数等于核外电子数,属于原子,最外层电子数是6,大于4,是最容易得到电子的原子;在⑥中,质子数=11>核外电子数=10,表示阳离子;微粒⑦的质子数是1,电子数是2,符号是:H-;③是硫离子,⑥是钠离自,二者形成化合物为硫化钠,化学式为Na2S;
(2)由上元素和常见物质的性质可知:含有+6价元素的酸是硫酸,化学式是:H2SO4,能与酸反应的氧化物是氧化钠,化学式是:Na2O,生活中重要的调味剂是氯化钠,化学式是:NaCl,含有三种元素的有机化合物有酒精等,化学式是:C2H5OH.
故答案为:(1)①;⑥;C;H-;Na2S;(2)H2SO4;Na2O;NaCl;C2H5OH.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
3.在某研究性学习小组调查发现,甲、乙两工厂排放的污水中含下列离子:H+、Cu2+、K+、NO3-、OH-中的三种离子(两厂含有一种相同的离子).若将两厂的污水按一定比例混合,沉淀后污水会变成无色澄清中性溶液.下列关于污水成分的分析,正确的是( )
| A. | H+和Cu2+来自同一工厂 | B. | Cu2+和K+来自同一工厂 | ||
| C. | H+和OH-来自同一工厂 | D. | OH-和Cu2-来自同一工厂 |
20.最近,科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰.电池总反应为:Zn+2MnO2+X═ZnO+2MnOOH.下列说法不正确的是( )
| A. | X为H2O | |
| B. | 该反应中MnO2为催化剂 | |
| C. | 该反应中共有3种氧化物 | |
| D. | 反应前后锌元素的化合价发生了变化 |


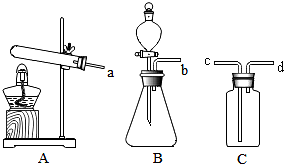 如图是实验室常用的制取气体的装置.
如图是实验室常用的制取气体的装置.