题目内容
17.小娜同学在实验室做了五组实验.分析并回答问题.
(1)A中试管振荡后所得溶液中溶质的化学式是C2H5OH.
(2)B组将试管振荡,倒掉液体,用水冲洗后,试管内壁是否都干净是(填“是”或“否”).
(3)C组试管中现象相同,写出右侧试管中反应的化学方程式Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(4)D组试管中都会产生白色沉淀,该组实验不能(填“能”或“不能”)体现酸的通性,写出右侧试管中反应的化学方程式BaCl2+H2SO4=BaSO4↓+2HCl.
(5)E的目的是测定空气中氧气含量,实验中下列操作不妥的是③④(填序号).
①检查装置气密性 ②实验前夹紧止水夹
③红磷熄灭即可打开止水夹 ④必须选用教室内的空气.
分析 (1)根据溶质溶剂分析;
(2)根据乳化作用分析;
(3)根据酸的通性分析;
(4)根据酸的通性分析;
(5)根据实验的注意事项分析.
解答 解:(1)A中试管振荡后所得溶液的溶质是乙醇,其的化学式是C2H5OH.
(2)B组将试管振荡,植物油遇到洗涤剂会发生乳化作用,倒掉液体,用水冲洗后,试管内壁干净,植物油属于酯类,在氢氧化钠作用下会水解为可溶性的醇和羧酸盐,倒掉液体,用水冲洗后,试管内壁干净;
(3)C组试管中现象相同,其原理都可用于除锈;写出右侧试管中反应是硫酸和氧化铁反应生成硫酸铁和水,反应的化学方程式是Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(4)D组试管中都会产生白色沉淀,盐酸和硝酸银反应产生氯化银沉淀和硝酸,氯化钡和硫酸反应产生硫酸钡沉淀和盐酸,反应的化学方程式分别为:AgNO3+HCl=AgCl↓+HNO3、BaCl2+H2SO4=BaSO4↓+2HCl,盐酸不能与氯化钡反应,所以该组实验不能体现酸的通性.
(5))E的目的是测定空气中氧气含量,实验中①检查装置气密性、②实验前夹紧止水夹、③红磷熄灭冷却到室温后再打开止水夹、④不一定选用教室内的空气.
故答案为:(1)C2H5OH;(2)是;(3)Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;(4)不能;BaCl2+H2SO4=BaSO4↓+2HCl;(5)③④.
点评 本题难度不大,掌握酸的化学性质(能与活泼金属、金属氧化物、碱、碳酸盐等反应)、物理性质并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
5.如图中四个选项中实验操作错误的是( )
| A. | 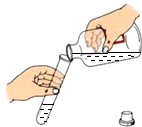 | B. |  | C. |  | D. |  |
12.小明在加热氯酸钾制氧气的实验中想加入二氧化锰作催化剂,不小心错加入了高锰酸钾,则结果会导致( )
| A. | 反应速率变快,最终生成氧气量增多 | |
| B. | 反应速率不变,最终生成氧气量增多 | |
| C. | 反应速率变快,最终生成氧气量不变 | |
| D. | 反应速率不变,最终生成氧气量不变 |
9.染发时常用到的着色剂--对苯二胺,是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其化学式为C6H8N2.有关对苯二胺的说法正确的是( )
| A. | 对苯二胺属于化合物 | |
| B. | 对苯二胺的相对分子质量为27 | |
| C. | 对苯二胺中碳、氢、氮元素的质量比为3:4:1 | |
| D. | 对苯二胺中碳.氢.氮原子个数比为18:2:7 |
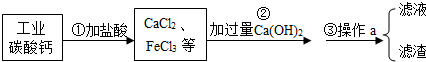
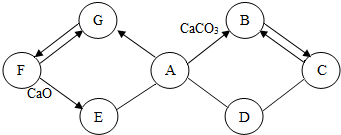 如图所示A~G是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知A是人体胃液中含有的酸,G是气体单质,B和C含有相同的元素.
如图所示A~G是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知A是人体胃液中含有的酸,G是气体单质,B和C含有相同的元素.