题目内容
7.有A、B、C、D、E五种实验装置,根据装置图回答下列问题(装置用序号表示):
(1)实验室制取氧气应选用的发生装置是A或B,若用E装置收集氧气时,气体应从a导气管通入瓶中.
(2)实验室制取二氧化碳应选用的发生装置是B,选用装置D除去二氧化碳中混有的少量水蒸气时,D内盛放的试剂应是浓硫酸.
(3)氨气(NH3)在通常状况下是一种无色有刺激性气味的气体,密度比空气的密度小,极易溶于水,其水溶液为氨水.实验室可用加热氯化铵和熟石灰两种固体混合物的方法制取氨气.
①实验室制取氨气应选用的发生装置是A,若用E装置收集氨气时,气体应从b导气管进入瓶中,因为氨气的密度比空气小.
②如图F所示,将一支装满氨气的试管倒放于水槽中可以观察到的现象是试管内液面上升,产生这种现象的原因是氨气极易溶于水.
分析 (1)依据实验室制取二氧化碳的反应物的状态和反应条件选择发生装置;浓硫酸具有吸水性,是一种常用的液体干燥剂;装置Ⅲ添加注射器可逐滴滴加液体,达到控制反应速率的目的;
(2)实验室制取氧气可用加热氯酸钾、高锰酸钾或过氧化氢常温分解的方法,然后依据发生装置的选择方法分析,并依据反应原理书写方程式;氧气的密度比空气大,故应从长导管进入,空气从短导管排出,更易排尽;
(3)①实验室可用加热氯化铵和熟石灰混合物的方法制取氨气,选用的发生装置;根据氨气的密度比空气小,进行解答;
②根据氨气密度比空气的密度小,极易溶于水,及压强的知识进行解答
解答 解:(1)实验室制取氧气若用加热氯酸钾的方法,则选发生装置A,若用过氧化氢常温分解的方法制取,则选装置B;氧气的密度比空气大,故应从长导管进入,空气从短导管排出,更易排尽;
(2)实验室制取二氧化碳用大理石与稀盐酸反应,不需加热,故选择发生装置B;浓硫酸D内盛放的试剂应是液体干燥剂浓硫酸;
(3))①实验室可用加热氯化铵和熟石灰混合物的方法制取氨气,选用的是“固体加热型”的发生装置为A;因为氨气的密度比空气小,用E装置收集氨气时,气体应从 b导气管进入瓶中;
②根据氨气极易溶于水,试管中氨气溶于水后,试管内压强减小,在大气压的作用下试管内液面上升;
故答案为:B、浓硫酸;
故答案为:(1)A或B;、a;
(2)B、浓硫酸;
(3)①A、氨气的密度比空气小、b;②试管内液面上升、氨气极易溶于水.
点评 本题考查学生根据实验室常见仪器和气体制取的反应原理,装置和相关气体的性质等,掌握相关知识才能正确分析解答.

练习册系列答案
相关题目
18.由于森林的过度砍伐、草场的大面积开垦,土地出现沙漠化,导致我国北方地区经常出现沙尘暴天气.请你预测当北京市出现沙尘天气时,首要污染物会是( )
| A. | 臭氧 | B. | 二氧化氮 | C. | 可吸入颗粒物 | D. | 二氧化硫 |
15.向铜粉和铁粉的混合物中加入一定量的盐酸,充分反应后过滤.以下判断不正确的是( )
| A. | 滤纸上可能没有铜 | B. | 滤纸上可能含有铁 | ||
| C. | 滤液中可能含有盐酸 | D. | 滤液中一定含有氯化亚铁 |
2.下列仪器使用不当的是( )
| A. | 用滴瓶盛放液体药品 | B. | 在量筒中配制食盐水 | ||
| C. | 在试管中进行化学反应 | D. | 用镊子夹取块状药品 |
12. 某课外小组研究“影响H2O2 生成O2快慢的因素”的课题.通过查阅资料,他们提出如下猜想.
某课外小组研究“影响H2O2 生成O2快慢的因素”的课题.通过查阅资料,他们提出如下猜想.
【提出猜想】催化剂和反应物浓度都会影响H2O2 生成O2的快慢
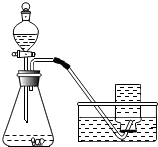
【实验过程】实验装置图如图:
实验操作:检查装置气密性良好.将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体.
实验记录
(1)H2O2溶液和二氧化锰制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)实验②中加入H2O2的体积为100mL.
(3)实验③中加入的固体和用量为0.5g二氧化锰.
【结论】该探究过程得出的结论是使用催化剂、增大反应物浓度可以加快H2O2生成O2的速度(或催化剂和反应物浓度都会影响H2O2生成O2的快慢);.
【反思】H2O2在常温下分解缓慢,加入MnO2后反应明显加快.小红提出,为了更好的证明二氧化锰和氯化钠是否对H2O2 生成O2快慢有影响,还应该增加一组对比实验.该实验选用的药品和用量为5%H2O2100mL(不加其他催化剂).
【实验拓展】小红用收集的气体进行氧气的性质实验.
(1)检验氧气的方法是将带火星的木条插入集气瓶中,木条复燃,证明集气瓶中为氧气.
(2)小红发现用该气体进行氧气的性质实验,现象都不明显.造成这种结果的原因是反应后首先排出的是锥形瓶中的空气,因此立即收集放出的气体中氧气纯度不高,导致铁丝无法在收集的气体中燃烧现象不明显.
 某课外小组研究“影响H2O2 生成O2快慢的因素”的课题.通过查阅资料,他们提出如下猜想.
某课外小组研究“影响H2O2 生成O2快慢的因素”的课题.通过查阅资料,他们提出如下猜想.【提出猜想】催化剂和反应物浓度都会影响H2O2 生成O2的快慢
【实验过程】实验装置图如图:
实验操作:检查装置气密性良好.将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体.
实验记录
| 实验编号 | ① | ② | ③ |
| 反应物 | 5%H2O2100mL | 5%H2O2 | 3%H2O2100mL |
| 加入固体 | 0.5g氯化钠固体 | 0.5g二氧化锰 | |
| 收集气体的时间 | 165s | 46s | 80s |
(2)实验②中加入H2O2的体积为100mL.
(3)实验③中加入的固体和用量为0.5g二氧化锰.
【结论】该探究过程得出的结论是使用催化剂、增大反应物浓度可以加快H2O2生成O2的速度(或催化剂和反应物浓度都会影响H2O2生成O2的快慢);.
【反思】H2O2在常温下分解缓慢,加入MnO2后反应明显加快.小红提出,为了更好的证明二氧化锰和氯化钠是否对H2O2 生成O2快慢有影响,还应该增加一组对比实验.该实验选用的药品和用量为5%H2O2100mL(不加其他催化剂).
【实验拓展】小红用收集的气体进行氧气的性质实验.
(1)检验氧气的方法是将带火星的木条插入集气瓶中,木条复燃,证明集气瓶中为氧气.
(2)小红发现用该气体进行氧气的性质实验,现象都不明显.造成这种结果的原因是反应后首先排出的是锥形瓶中的空气,因此立即收集放出的气体中氧气纯度不高,导致铁丝无法在收集的气体中燃烧现象不明显.
19.在太空舱里,为了保持舱内CO2气体含量的相对稳定,常用NiFe2O4作催化剂将宇航员呼出的CO2转化为O2.NiFe2O4中铁元素的化合价为+3价,则Ni的化合价为( )
| A. | +2 | B. | +1 | C. | +3 | D. | +4 |
16.金属活动性顺序:K Ca Na Mg Al ZnFeSn Pb(H)CuHg Ag Pt Au,请你在横线上填写对应金属的元素符号.猜想1.Cr>Fe>Cu;2.Fe>Cu>Cr;3.你的猜想是Fe>Cr>Cu.
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
(1)得到的结论是猜想1正确.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 | 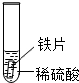 | 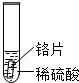 |  |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | 无现象 |
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
6.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,向滤渣中滴加稀盐酸,产生气泡,有关判断正确的是( )
| A. | 滤液中一定有硝酸锌、硝酸铜、硝酸银 | |
| B. | 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银 | |
| C. | 滤液中一定有银、铜和锌 | |
| D. | 滤液中一定有银和锌,可能有铜 |