题目内容
1.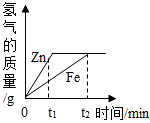 一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法正确的是( )
一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法正确的是( )| A. | t1时,产生氢气的质量锌比铁小 | B. | t1时,产生氢气的速率锌比铁大 | ||
| C. | t2时,参加反应锌的质量与铁相同 | D. | t2时,锌、铁消耗的盐酸质量相同 |
分析 根据题意“将一定质量的锌和铁分别放入等量的稀盐酸中”,通过图象可知金属锌和铁与酸反应的速率和生成氢气的质量,由此可推出金属活动性顺序,并结合化学方程式的计算可推出金属和酸的用量问题.
解答 解:A、由图象可知,t1时,产生氢气的质量锌比铁大.故A说法错误;
B、t1时,产生氢气的质量锌比铁大.所以,产生氢气的速率锌比铁大.故B说法正确;
C、t2时,生成的氢气的质量相同,根据Zn~H2和Fe~H2,可知65gZn生成2g氢气,56gFe生成2g氢气,因此参加反应锌的质量与铁不同,故C说法错误;
D、t2时,生成的氢气的质量相同,锌、铁消耗的盐酸质量相同.故D说法正确.
故选BD.
点评 本题考查金属与酸反应的有关知识,综合性较强,不仅需要根据图象和题意分析出直接信息,还需要根据计算得出用量问题.

练习册系列答案
相关题目
2.下列物质常用于实验室制取二氧化碳的是( )
| A. | 大理石和稀硫酸 | B. | 石灰石和稀盐酸 | ||
| C. | 碳酸钠和稀盐酸 | D. | 碳酸氢钠和稀盐酸 |
9.过氧化氢溶液在放置的过程中会慢慢地分解,某200g含氧元素89.3%的过氧化氢水溶液放置一段时间后,经试验测定已变成纯净物,则放置该过程中产生氧气的质量为( )
| A. | 9.8g | B. | 15.1g | C. | 3.7g | D. | 7.4g |
16.仓库中有一包氮肥的包装标签模糊不清,有同学进行了以下探究: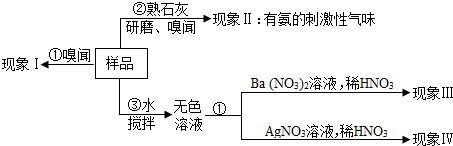
(1)操作③用玻棒搅拌的目的是使样品充分溶解.
(2)请完成下表(已知AgCl和BaSO4是难溶于水和酸的白色固体):
(3)若现象Ⅲ、Ⅳ都无现象,则该氮肥可能是NH4NO3(写化学式);若操作②现象为无气味、现象Ⅲ、Ⅳ无现象,则该氮肥可能是尿素(只写一种).

(1)操作③用玻棒搅拌的目的是使样品充分溶解.
(2)请完成下表(已知AgCl和BaSO4是难溶于水和酸的白色固体):
| 项目 | 假设和现象 | 判断和化学方程式 |
| a | 若现象I为无氨味 | 则样品中不含碳酸氢铵(填名称) |
| b | 由操作②现象判断 | 该样品一定含有铵根离子 |
| c | 若现象Ⅲ为白色沉淀,现象Ⅳ为无沉淀 | 则样品中含有硫酸铵(写名称) |
| d | 若现象Ⅲ为无沉淀,现象Ⅳ为白色沉淀 | 则样品中含有NH4Cl(写化学式) 该反应的化学方程式为:NH4Cl+AgNO3═AgCl↓+NH4NO3 |
6.用数轴表示某些化学知识直观、简明、易记.下列数轴表示的化学知识不正确的是( )
| A. |  金属活动性由弱到强 | |
| B. |  液体的pH值由低到高 | |
| C. |  氯元素的化合价由低到高 | |
| D. |  常温常压下气体在水中的溶解性由弱到强 |
13.某氯化钠溶液中含有少量的氯化钡和氢氧化钠溶液杂质,它们的质量比为13:10.欲将两种杂质同时除去,得到纯净的氯化钠溶液,可选用的试剂组合是( )
| A. | 盐酸和硫酸溶液,其溶质的质量比为73:49 | |
| B. | 盐酸和硫酸钠溶液,其质量比为73:71 | |
| C. | 硫酸和硫酸钠溶液,其质量比为98:71 | |
| D. | 硫酸和硫酸镁溶液,其溶质的质量比为49:60 |
10.下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而增大的是( )
| A. | 浓盐酸 | B. | 氯化钠溶液 | C. | 氢氧化钠溶液 | D. | 浓硫酸 |
11.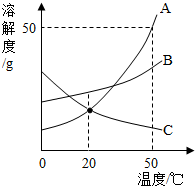 如图是A、B、C三种固体的溶解度曲线.下列分析不正确的是( )
如图是A、B、C三种固体的溶解度曲线.下列分析不正确的是( )
 如图是A、B、C三种固体的溶解度曲线.下列分析不正确的是( )
如图是A、B、C三种固体的溶解度曲线.下列分析不正确的是( )| A. | 50℃时,三种物质的溶解度由大到小的顺序是A>B>C | |
| B. | 50℃时,把50g A放入50g水中,形成的溶液其中溶质与溶剂的质量比为1:2 | |
| C. | 将C的饱和溶液变为不饱和溶液,可采用降温的方法 | |
| D. | 分别将三种物质的饱和溶液从50℃将至20℃时,所得溶液溶质质量分数大小关系是B>C=A |