题目内容
镁与盐酸(HCl)反应生成氢气和氯化镁.
(1)写出该反应的化学方程式 .
(2)实验室里用2.4g镁与足量盐酸反应,可制得氢气和氯化镁的质量各是多少?
(1)写出该反应的化学方程式
(2)实验室里用2.4g镁与足量盐酸反应,可制得氢气和氯化镁的质量各是多少?
考点:根据化学反应方程式的计算,书写化学方程式、文字表达式、电离方程式
专题:有关化学方程式的计算
分析:由镁和盐酸反应生成氯化镁和氢气,写出反应的化学方程式,进而根据镁的质量计算出制得氢气和氯化镁的质量;
解答:解:(1)镁和盐酸反应生成氯化镁和氢气,反应的化学方程式为Mg+2HCl═MgCl2 +H2↑
(2)设,可制得氢气质量为x,和氯化镁质量为y,
Mg+2HCl═MgCl2 +H2↑
24 95 2
2.4g y x
=
=
,
x=0.2g,y=9.5g
答案:(1)Mg+2HCl═MgCl2 +H2↑
(2)可制得氢气质量为0.2克,氯化镁质量为9.5克.
(2)设,可制得氢气质量为x,和氯化镁质量为y,
Mg+2HCl═MgCl2 +H2↑
24 95 2
2.4g y x
| 24 |
| 2.4g |
| 95 |
| y |
| 2 |
| x |
x=0.2g,y=9.5g
答案:(1)Mg+2HCl═MgCl2 +H2↑
(2)可制得氢气质量为0.2克,氯化镁质量为9.5克.
点评:本题难度不大,掌握根据化学方程式的有关计算并能灵活运用即可正确解答本题.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
小晴同学为了探究氨气(NH3)的性质,做了如图所示的实验:请根据小晴的操作和相关现象分析下列描述错误的是( )


| A、①氨气的密度比空气小 |
| B、②氨气溶于水使试管内压强减小 |
| C、③试管内液体的PH<7 |
| D、④若将酚酞试剂改为石蕊溶液可看到蓝色喷泉 |
最近很多城市频发“雾霾”天气,空气中PM2.5含量升高,对人的呼吸系统造成了一定的伤害.雾霾现象主要与下列哪种物质有关( )
| A、氮气 | B、一氧化碳 |
| C、二氧化碳 | D、可吸入颗粒物 |
近来许多饮品被曝“塑化剂”超标.邻苯二甲酸二辛酯(化学式为C24H38O4)是一种常见的“塑化剂”.下列说法中正确的是( )
| A、该塑化剂属于氧化物 |
| B、该塑化剂中碳元素的质量分数最大 |
| C、该塑化剂中碳、氧元素质量比为6:1 |
| D、该塑化剂由24个碳原子、38个氢原子、4个氧原子构成 |
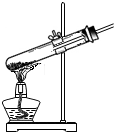 基本操作:
基本操作: