题目内容
6.取4.8g镁与100g稀硫酸恰好完全反应后得到无色溶液,试计算:稀硫酸中溶质的质量分数?分析 镁与稀硫酸反应生成硫酸镁和氢气;根据参加反应的镁的质量,由反应的化学方程式列式计算出稀硫酸的溶质的质量,进而计算出溶质的质量分数.
解答 解:设稀硫酸中溶质的质量为x,
Mg+H2SO4═MgSO4+H2↑
24 98
4.8g x
$\frac{24}{98}=\frac{4.8g}{x}$ 解得:x=19.6g
稀硫酸的溶质质量分数为$\frac{19.6g}{100g}×100%$=19.6%.
答:稀硫酸的溶质质量分数为19.6%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案
相关题目
16.下面四个家庭小实验,不能制得溶液的是( )
| A. | 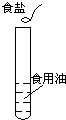 | B. | 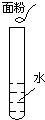 | C. | 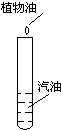 | D. | 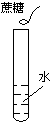 |
17.化学反应往往需要在一定的条件下进行.通过控制或改变反应条件可以加快、减缓甚至组织反应的行.下列所反映的措施中,能加快其化学反应速率的是( )
| A. | 铁门表面喷漆 | |
| B. | 冰箱保存食物 | |
| C. | 用扇子扇煤炉火,火会更旺 | |
| D. | 将木头电线杆埋入地下的部分用火微微烧焦 |
14.一瓶气体经过化验得知其中只有一种元素,则该气体是( )
| A. | 一种单质 | |
| B. | 单质、化合物的混合物 | |
| C. | 一种化合物 | |
| D. | 既可能是一种单质,也可能是几种单质的混合物 |
1.若1.6g某物质完全燃烧生成4.4gCO2和3.6gH2O,则该物质含有的元素为( )
| A. | C、H、O三种元素 | B. | C、H两种元素 | C. | C、O两种元素 | D. | O、H两种元素 |
11.室温下,饱和食盐水露置在干燥的空气中,过一段时间后有少量固体析出,这是因为( )
| A. | 氯化钠的溶解度减小了 | B. | 溶液中溶质的质量分数减小了 | ||
| C. | 溶剂质量减小了 | D. | 溶液变成不饱和溶液了 |
15.实验室制取氢气常用的药品是( )
| A. | 浓硫酸和锌 | B. | 稀硫酸和锌 | C. | 浓盐酸和锌 | D. | 硝酸和铁 |