题目内容
阅读资料:
(1)氨气(NH3)具有还原性,可以还原氧化铜,生成铜、氮气和水;
(2)实验室制氨气:2NH4Cl + Ca(OH)2  CaCl2 + 2NH3↑ + 2H2O
CaCl2 + 2NH3↑ + 2H2O
(3)白色的无水硫酸铜遇水会变成蓝色,可以用于检测微量水的存在;
(4)碱石灰可以吸收水分,可以干燥氨气;
利用氨气还原氧化铜的反应,可设计测定铜元素相对原子质量近似值的实验。原理是先称量反应物氧化铜的质量,反应完全后测定生成物水的质量,由此计算铜元素相对原子质量。为此设计了下列实验装置(图中部分夹持仪器省略,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
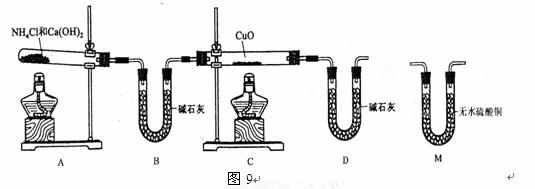
|
请回答下列问题
(1)写出氨气还原氧化铜的化学方程式
(2)B装置的作用是
D装置的作用是 __________
(3)为了确认没有水进入C装置中,需在整套装置中添加装置M于 (选填序号)。
a. A-B间 b. B-C间 c.C-D间
(4)在本实验中,若测得水的质量为a g,反应物氧化铜的质量为b g,则铜元素的相对原子质量是____。
(5)在本实验中,还可通过测定______和_____的质量,达到实验目的。
 名校课堂系列答案
名校课堂系列答案苏州博物馆最近启用新购置的“真空充氮杀虫灭菌消毒机”来处理和保护文物,即将文物置于该机器内,三天后氮气浓度可达99.99%;再密闭三天左右,好氧菌、厌氧菌和丝状霉菌都被杀灭.下列有关氮气说法错误的是( )
|
| A. | 高浓度氮气可抑制菌类的生长 | B. | 氮气不能供给呼吸 |
|
| C. | 通常情况下氮气的化学性质不活泼 | D. | 通常状况下氮气易溶于水 |
下列不属于氧化物的是( )
|
| A. | 二氧化锰 | B. | 五氧化二磷 | C. | 高锰酸钾 | D. | 过氧化氢 |


 选择正确的填入下列空格内:
选择正确的填入下列空格内: 深井中可能积存有大量
深井中可能积存有大量 的 ,
的 , )
)