题目内容
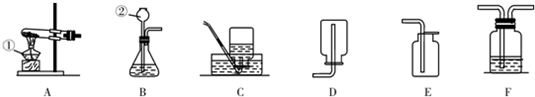
4.实验室常用的干燥剂“碱石灰”是CaO和固体NaOH的混合物,极易与空气中水蒸汽和CO2反应而变质.某同学对一瓶久置的“碱石灰”作了如下探究:(1)【猜想】
猜想Ⅰ:没有变质,“碱石灰”只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和Na2CO3.
则CaO与水反应的反应方程式为CaO+H2O═Ca(OH)2.
(2)【实验】如图所示:
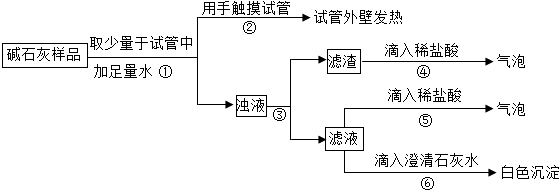
(3)a.若Ca(OH)2、CaCO3和Na2CO3投入到水中不会放热,则由操作②现象判断:猜想Ⅱ不成立(填:“成立”或“不成立”).
b.操作④发生化学反应的方程式为CaCO3+2HCl═CaCl2+CO2↑+H2O;由操作⑤⑥的现象判断:滤液中含有Na2CO3(写化学式);由此判断猜想Ⅰ不成立(填:“成立”或“不成立”).
c.综合a和b的结论,判断该样品变质情况为部分变质.
(4)【反思】有同学认为,不进行操作④,也可判断滤渣一定为CaCO3,你认为该同学的看法是错误(填“正确”或“错误”)的,理由是氢氧化钙微溶于水.由上述实验说明,实验室中“碱石灰”应密封保存.
分析 根据已有的知识进行分析解答,氧化钙能与水反应生成氢氧化钙且放出热量,碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,滤液中加入盐酸产生气泡,能与氢氧化钙反应产生白色沉淀,说明含有碳酸钠,据此解答.
解答 解:(1)氧化钙能与水反应生成氢氧化钙,故填:CaO+H2O═Ca(OH)2;
(3)a、氧化钙能与水反应放出热量,试管壁发热说明含有氧化钙,故猜想Ⅱ不成立,故填:不成立;
b、滤渣中加入盐酸产生气体,说明滤渣中含有碳酸钙,碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,滤液中加入盐酸产生气泡,能与氢氧化钙反应产生白色沉淀,说明含有碳酸钠,故猜想Ⅰ不成立,故填:CaCO3+2HCl═CaCl2+CO2↑+H2O;Na2CO3;不成立;
c、样品中含有氧化钙,含有碳酸钙和碳酸钠,说明药品是部分变质,故填:部分变质.
(4)不进行操作④,无法判断滤渣一定为CaCO3,因为氢氧化钙微溶于水;碱石灰在空气中极易变质,所以需要密封保存;故填:错误;氢氧化钙微溶于水;密封;
点评 本题考查的是变质药品成分的实验探究,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
14.下列现象中,只发生物理变化的是( )
| A. | 玻璃破碎 | B. | 牛奶变质 | C. | 木炭燃烧 | D. | 铁丝生锈 |
9.在生活中经常曝出某品牌金饰品掺假的事件,引起学生的好奇,某化学兴趣小组在老师的帮助下,对几种常见金属饰品所含的金属进行了相关的探究活动.
【提出问题】(1)怎样鉴别真假黄金?(2)怎样确定钯的金属活动性?
【查阅资料】(1)假黄金通常是黄铜(Cu-Zu合金) (2)钯(Pd)呈银白色,有金属光泽,可用作饰品
【实验药品 钯、铂(Pt)、稀盐酸、硝酸银溶液和氯化钯(PdCl2)溶液
【实验探究】(1)鉴别黄金样品的真假:取黄金样品于试管中,滴加稀盐酸后,观察黄金样品表面有气泡产生,该气体是氢气(填名称),说明此样品为假(填“真”或“假”)黄金.
(2)探究钯的金属活动性:依据生活经验,同学们猜测钯的活动性可能与银和铂相近,于是他们利用上述药品进行如下实验:
初步得出结论:钯、银、铂的金属活动性由强到弱的顺序为银>钯>铂.
【废液处理】(1)转化成沉淀.小组同学所有液体倒入废液缺缸中,出现白色沉淀.写出产生该现象的化学方程式:ZnCl2+2AgNO3=2AgCl↓+Zn(NO3)2(写出一个即可).
(2)通过科学合理的方法进一步回收金属钯.
【提出问题】(1)怎样鉴别真假黄金?(2)怎样确定钯的金属活动性?
【查阅资料】(1)假黄金通常是黄铜(Cu-Zu合金) (2)钯(Pd)呈银白色,有金属光泽,可用作饰品
【实验药品 钯、铂(Pt)、稀盐酸、硝酸银溶液和氯化钯(PdCl2)溶液
【实验探究】(1)鉴别黄金样品的真假:取黄金样品于试管中,滴加稀盐酸后,观察黄金样品表面有气泡产生,该气体是氢气(填名称),说明此样品为假(填“真”或“假”)黄金.
(2)探究钯的金属活动性:依据生活经验,同学们猜测钯的活动性可能与银和铂相近,于是他们利用上述药品进行如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 把钯浸入硝酸银溶液中 | 无明显现象 | 钯的活动性比银弱 |
| 把铂浸入氯化钯溶液中 | 无明显现象 | 钯的活动性比铂强 |
【废液处理】(1)转化成沉淀.小组同学所有液体倒入废液缺缸中,出现白色沉淀.写出产生该现象的化学方程式:ZnCl2+2AgNO3=2AgCl↓+Zn(NO3)2(写出一个即可).
(2)通过科学合理的方法进一步回收金属钯.