题目内容
11.取16g某有机化合物在氧气中完全燃烧,生成22g二氧化碳和18g水.(1)在该有机物中,含碳元素和氢元素的质量为多少?
(2)该化合物中是否含有氧元素?若有,质量为多少?若没有,请说明理由.
(3)若该有机物的相对分子质量为32,那么其化学式是什么?并写出该有机物在空气中燃烧的化学方程式.
分析 根据质量守恒定律可知:生成二氧化碳中碳元素的质量等于该化合物中碳元素的质量;生成的水中氢元素的质量等于该化合物中氢元素的质量;其余则为氧元素的质量.根据该化合物的元素质量比就可以确定其的化学式.
解答 解:(1)22g二氧化碳中含有的碳元素的质量为:22g×$\frac{12}{44}×100%$=6g;
18g水中含有的氢元素的质量为:18g×$\frac{1×2}{18}×100%$=2g;
故答案为:在该有机物中,含碳元素和氢元素的质量分别为6g、2g;
(2)有机物中碳元素和氢元素的质量和为:6g+2g=8g,所以有机物中含有氧元素,并且氧元素的质量为:16g-8g=8g.故答案为:有,氧元素的质量为8g;
(3)设该化合物的化学式为CXHYOZ.根据有机物中,碳元素、氢元素、氧元素的质量比为:3:1:4,和有机物相对分子质量为32,则有:12X=32×$\frac{3}{8}$,Y=32×$\frac{1}{8}$,16Z=32×$\frac{4}{8}$,解得:X=1,Y=4,Z=1,有机物的化学式是CH3OH.其燃烧生成水和二氧化碳,故填:2CH3OH+2O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O.
点评 物质在氧气中完全燃烧,产物只有二氧化碳和水.根据化学反应前后元素的种类和质量都不变,则生成的二氧化碳中碳元素的质量就是物质中碳元素的质量;生成的水中氢元素的质量就是物质中氢元素的质量.若碳元素与氢元素的质量和等于物质质量,则物质中不含氧元素;若小于物质质量,则物质中含有氧元素.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
1.下列说法正确的是( )
| A. | 20℃,100gNaCl饱和溶液中含有36gNaCl,则该温度下NaCl的溶解度为36g | |
| B. | NaCl的饱和溶液一定比NaCl的不饱和溶液浓 | |
| C. | 向15g10%的NaCl溶液加入15g水后,溶液中NaCl的质量分数一定为5% | |
| D. | 降低温度一定能使不饱和的NaCl溶液变为饱和的NaCl溶液 |
2.梧州市的“六堡茶”畅销全国各地,“茶香阵阵”这是因为( )
| A. | 分子在不断运动 | B. | 分子质量很小 | C. | 分子间有间隔 | D. | 分子可以再分 |
8.下列物质的用途中,利用其化学性质的是( )
(1)酒精用作燃料 (2)氢气(密度最小的气体)用于填充探空气球
(3)氧气用于气焊 (4)干冰用作致冷剂 (5)熟石灰改良酸性土壤.
(1)酒精用作燃料 (2)氢气(密度最小的气体)用于填充探空气球
(3)氧气用于气焊 (4)干冰用作致冷剂 (5)熟石灰改良酸性土壤.
| A. | (1)(2)(3) | B. | (1)(3)(5) | C. | (3)(4)(5) | D. | (1)(4)(5) |
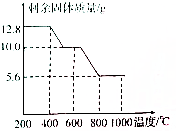 草酸钙(CaC2O4)是一种难溶于水的白色固体,受热能分解:CaC2O4$\frac{\underline{\;400~500℃\;}}{\;}$CaCO3+CO↑.为了探究其在加热条件下发生的变化,进行如下实验:取12.8g草酸钙固体在不断加热的条件下测得剩余固体的质量与温度的关系如图所示.
草酸钙(CaC2O4)是一种难溶于水的白色固体,受热能分解:CaC2O4$\frac{\underline{\;400~500℃\;}}{\;}$CaCO3+CO↑.为了探究其在加热条件下发生的变化,进行如下实验:取12.8g草酸钙固体在不断加热的条件下测得剩余固体的质量与温度的关系如图所示.
 某同学在实验室发现一瓶标签残缺的溶液(如图甲所示).为了测定此溶液的溶质质量分数,他取出30克该溶液,向其中逐滴加入溶质质量分数为20%的NaOH溶液.反应过程中生成沉淀的质量与所用NaOH溶液质量的关系如图乙所示.请计算此溶液的溶质质量分数.
某同学在实验室发现一瓶标签残缺的溶液(如图甲所示).为了测定此溶液的溶质质量分数,他取出30克该溶液,向其中逐滴加入溶质质量分数为20%的NaOH溶液.反应过程中生成沉淀的质量与所用NaOH溶液质量的关系如图乙所示.请计算此溶液的溶质质量分数.