题目内容
19.在196克稀硫酸中加入32.5克锌粒,两者恰好完全反应,求:(1)生成的气体的质量
(2)反应后溶液中溶质的质量分数.
分析 锌和稀硫酸反应生成硫酸锌和氢气,根据反应的化学方程式就提供的数据可以进行相关方面的计算和判断.
解答 解:(1)设反应生成硫酸锌质量为x,生成氢气的质量为y,
Zn+H2SO4═ZnSO4+H2↑,
65 161 2
32.5g x y
$\frac{65}{32.5}$=$\frac{161}{x}$=$\frac{2}{y}$,
x=80.5g,y=1g,
答:生成了1g氢气.
(2)反应后溶液中溶质的质量分数为:$\frac{80.5g}{196g+32.5g-1g}$×100%=35.4%,
答:反应后溶液中溶质的质量分数为35.4%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列物质中能与氢氧化钠溶液发生反应,有蓝色絮状沉淀的是( )
| A. | 氯化铁溶液 | B. | 酚酞试液 | C. | 稀盐酸 | D. | 硫酸铜溶液 |
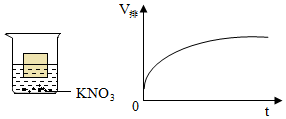 20℃时,分别向盛有10g水的A、B两支试管中加入等质量的甲、乙两种固体,充分溶解后,观察到如图1所示的现象.图2表示的甲乙两种物质的溶解度曲线.
20℃时,分别向盛有10g水的A、B两支试管中加入等质量的甲、乙两种固体,充分溶解后,观察到如图1所示的现象.图2表示的甲乙两种物质的溶解度曲线. 水和溶液在生命活动和生产、生活中起着十分重要的作用.
水和溶液在生命活动和生产、生活中起着十分重要的作用. 如图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:欲配制20%的稀盐酸1000g,需要用这种盐酸和水(水的密度为1.0g/cm3)各多少毫升?(结果精确到0.1mL)
如图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:欲配制20%的稀盐酸1000g,需要用这种盐酸和水(水的密度为1.0g/cm3)各多少毫升?(结果精确到0.1mL)