题目内容
2.下列图示是20℃时,向一定量的水中不断加入蔗糖固体充分溶解的过程图,对此溶解过程形成的溶液判断中不合理的是( )| A. |  属于不饱和溶液 | B. |  属于不饱和溶液 | C. |  属于饱和溶液 | D. |  属于饱和溶液 |
分析 溶液中存在不溶解的溶质,说明在该温度下,该溶液是该种溶质的饱和溶液.
解答 解A、A中加入蔗糖后,全部溶解,在B中继续加入蔗糖还能溶解,说明A中溶液是不饱和溶液,故A说法正确;
B、B中加入一定质量的蔗糖,全部溶解,此时的溶液可能是不饱和溶液,也可能恰好变为饱和溶液,故B说法错误;
C、C烧杯中含有不溶解的蔗糖,所以该溶液属于饱和溶液,故C说法正确;
D、D烧杯中含有不溶解的蔗糖,所以该溶液属于饱和溶液,故D说法正确.
故选B.
点评 解答本题关键是知道溶液是否饱和的判断方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.在中央电视台发布的重点城市空气质量日报中可看到,造成空气污染的首要污染物是可吸入颗粒物和二氧化硫,下列对其形成主要原因的分析不合理的是( )
| A. | 环境绿化不好粉尘随风飘扬 | B. | 生活和生产中燃烧煤炭 | ||
| C. | 工业生产排放废水 | D. | 机动车排放尾气 |
10.下列关于空气的说法正确的是( )
| A. | N2、O2体积比约为5:1 | B. | N2、O2等均匀地混合 | ||
| C. | 空气由空气分子构成 | D. | N2、O2不再保持各自的化学性质 |
7.质量守恒定律的发现对化学的发展做出了重要贡献.
(1)为研究化学反应前后反应物和生成物之间的质量关系,同学们在实验室做了下列三个实验.
实验一:称量镁条,在空气中点燃镁条,待反应结束后,再称量得到的固体.
实验二:将盛有稀盐酸的小试管放入装有石灰石的烧杯中,一起称量,然后将盐酸和石灰水混合,充分反应后一起称量.
实验三:将盛有氢氧化钠溶液的试管放入盛有硫酸铜溶液的烧杯中,一起称量,然后使两种溶液混合,充分反应后再一起称量.
三个实验得到的实验数据如下表:
①实验一的反应现象为镁条燃烧,发出耀眼的白光,放热,生成白色固体,反应的化学方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.但往往在实验结束后再次称量固体时,发现固体质量比反应前减小,可能的原因是镁带燃烧时有一缕白烟(为生成的氧化镁)向空气中扩散,造成氧化镁的损失;镁带燃烧时夹镁带的坩埚钳上有-层白色粉末,此粉末为氧化镁,也造成氧化镁的损失.
②由表中数据分析,实验中反应前后质量不相等的原因是实验中没有称量反应物氧气的质量.
(2)将50g酒精和50g水混合后总质量为100g,说明该实验也能验证质量守恒定律,这种说法是否正确?不正确,理由是因为两种物质未参加化学反应,所以不能验证质量守恒定律.
(1)为研究化学反应前后反应物和生成物之间的质量关系,同学们在实验室做了下列三个实验.
实验一:称量镁条,在空气中点燃镁条,待反应结束后,再称量得到的固体.
实验二:将盛有稀盐酸的小试管放入装有石灰石的烧杯中,一起称量,然后将盐酸和石灰水混合,充分反应后一起称量.
实验三:将盛有氢氧化钠溶液的试管放入盛有硫酸铜溶液的烧杯中,一起称量,然后使两种溶液混合,充分反应后再一起称量.
三个实验得到的实验数据如下表:
| 实验序号 | 实验一 | 实验二 | 实验三 |
| 反应前(g) | 4.8 | 116.8 | 118.4 |
| 反应后(g) | 8.0 | 112.4 | 118.4 |
②由表中数据分析,实验中反应前后质量不相等的原因是实验中没有称量反应物氧气的质量.
(2)将50g酒精和50g水混合后总质量为100g,说明该实验也能验证质量守恒定律,这种说法是否正确?不正确,理由是因为两种物质未参加化学反应,所以不能验证质量守恒定律.
14.日常生活中的下列物质属于纯净物的是( )
| A. |  雪碧汽水 | B. |  | ||
| C. |  | D. |  |
11.张老师与同学们探究化学反应前后物质的质量关系,现请你一同参与:
【提出问题】化学反应前后物质的质量总和是否相等?
【猜想假设】猜想1:各物质的质量总和不相等; 猜想2:各物质的质量总和相等.
【实验探究】同学们根据实验方案分组实验,用托盘天平分别称量反应前后物质的质量
【分组实验一】将打磨干净的铁钉浸入CuSO4溶液中,实验现象为铁钉表面有红色物质析出,待溶液颜色发生改变时,再次称量,结果天平指针没有偏转.
【分组实验二】稀盐酸与碳酸钠粉末反应的实验现象为有气泡产生,天平指针向右偏转.
【评价与反思】究竟哪种猜想正确?同学们分析两个方案的实验结果,通过讨论一致认为:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在密闭容器(或封闭体系等)中进行.
【得出结论】同学们进一步分析发现,反应体系中仪器和未参加反应的物质质量在反应前后保持不变,最终得出结论:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和.即猜想2正确.
【提出问题】化学反应前后物质的质量总和是否相等?
【猜想假设】猜想1:各物质的质量总和不相等; 猜想2:各物质的质量总和相等.
【实验探究】同学们根据实验方案分组实验,用托盘天平分别称量反应前后物质的质量
| 实验方案一 | 实验方案二 |
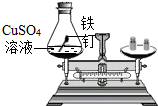 | 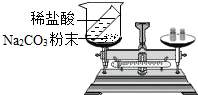 |
【分组实验二】稀盐酸与碳酸钠粉末反应的实验现象为有气泡产生,天平指针向右偏转.
【评价与反思】究竟哪种猜想正确?同学们分析两个方案的实验结果,通过讨论一致认为:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在密闭容器(或封闭体系等)中进行.
【得出结论】同学们进一步分析发现,反应体系中仪器和未参加反应的物质质量在反应前后保持不变,最终得出结论:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和.即猜想2正确.
 A~H都是初中化学中常见的物质,已知A、B为黑色固体,C为气体,D为红色固体单质,F为红色固体化合物,它们的转化关系如图所示.请回答:
A~H都是初中化学中常见的物质,已知A、B为黑色固体,C为气体,D为红色固体单质,F为红色固体化合物,它们的转化关系如图所示.请回答: