题目内容
5.铁是自然界中分布最广的元素之一,但大都以化合态存在于地壳中,冶金工业上是用铁矿石、焦炭、石灰石为原料,在高炉内冶炼而获得铁.高炉内的反应相当复杂,主要反应可表示为Fe2O3+3CO═2Fe+3CO2.科学上将化学反应后化合价升高的元素对应的反应物称为还原剂,化学反应后化合价降低的元素对应的反应物称为氧化剂.该化学反应中的还原剂是CO,100吨含Fe2O3的质量分数为80%的铁矿石,可冶炼出含铁96%的生铁58吨.(保留整数)分析 由赤铁矿石的质量、氧化铁的质量分数、生铁中铁的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出炼出生铁的质量.
解答 解:对于反应Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2中,CO中C的化合价由+2价,升高到CO2中+4价,是该化学反应中的还原剂;
设理论上可炼出含铁96%的生铁质量为x.
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
100t×80% 96%x
$\frac{160}{100t×80%}=\frac{112}{96%x}$
x=58t
答案:CO;58t
点评 本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
15.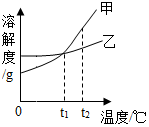 如表是NaCl、NH4Cl在不同温度时的溶解度.
如表是NaCl、NH4Cl在不同温度时的溶解度.
(1)如图表示氯化铵溶解度曲线的是甲(填甲或者乙).
(2)t1的范围为0~20
(3)将t2℃等质量的两种物质的饱和溶液降温至t1℃,对所得溶液的叙述正确的③④⑤(填序号).
①溶质质量分数:甲>乙 ②溶液质量:甲>乙
③所含溶剂质量:甲<乙 ④甲、乙都是饱和溶液 ⑤溶质质量:甲<乙
(4)t2℃等质量的两种物质配置成饱和溶液所得溶液的质量甲<乙(填><或=)
 如表是NaCl、NH4Cl在不同温度时的溶解度.
如表是NaCl、NH4Cl在不同温度时的溶解度.| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | |
(2)t1的范围为0~20
(3)将t2℃等质量的两种物质的饱和溶液降温至t1℃,对所得溶液的叙述正确的③④⑤(填序号).
①溶质质量分数:甲>乙 ②溶液质量:甲>乙
③所含溶剂质量:甲<乙 ④甲、乙都是饱和溶液 ⑤溶质质量:甲<乙
(4)t2℃等质量的两种物质配置成饱和溶液所得溶液的质量甲<乙(填><或=)
20.物质王国发生了一起团伙盗窃案,“警察”把三名“嫌疑犯”(分别是稀硫酸、氯化钠溶液和石灰水)带回了“警察局”.上级派出下列四名“警察”分别去审问“他们”(即把“他们”鉴别出来).能完成任务的“警察”是( )
| A. |  紫色石蕊试液“警察” | B. |  稀盐酸“警察” | ||
| C. |  无色酚酞试液“警察” | D. |  水“警察” |
10.下列图片中,不属于模型的是( )
| A. |  演播室的“嫦娥三号” | B. |  交通标志 | ||
| C. |  地球仪 | D. |  甲烷分子 |
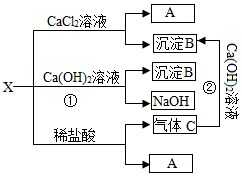 X是常见固态化合物,可发生如图所示的变化
X是常见固态化合物,可发生如图所示的变化 回答以下生活中的化学知识.
回答以下生活中的化学知识.