题目内容
13.将足量的氧化铜和木炭粉末均匀混合,隔绝空气加强热,充分反应后所得固体的质量比原混合物减少了8.8g.则原混合物中有多少克氧化铜?分析 依据2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑可知,该反应中反应前后固体减少的质量就是生成二氧化碳的质量,所以利用方程式中二氧化碳的质量可以求出原混合物中氧化铜的质量.
解答 解:由反应的情况可知该反应中反应前后固体减少的质量就是生成二氧化碳的质量,其质量是8.8g.
设原混合物中氧化铜的质量为x
2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑
160 44
x 8.8g
$\frac{160}{x}=\frac{44}{8.8g}$
解得:x=32g
答:原混合物中氧化铜的质量为32g.
点评 此题是对化学方程式计算的考查,解题的关键是分析出生成的二氧化碳的质量,进而依据方程式计算的基本步骤即可解决问题.

练习册系列答案
相关题目
1.下列物质间的转化都能通过一步反应实现的是( )


| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
14. 4月22日是“世界地球日”,如图是中国邮政发行的世界地球日邮票,号召人们关爱地球.下列行为中不利于地球保护的是( )
4月22日是“世界地球日”,如图是中国邮政发行的世界地球日邮票,号召人们关爱地球.下列行为中不利于地球保护的是( )
 4月22日是“世界地球日”,如图是中国邮政发行的世界地球日邮票,号召人们关爱地球.下列行为中不利于地球保护的是( )
4月22日是“世界地球日”,如图是中国邮政发行的世界地球日邮票,号召人们关爱地球.下列行为中不利于地球保护的是( )| A. | 研发可降解塑料或替代用品,控制白色污染 | |
| B. | 严格履行《京都议定书》,控制温室气体的排放 | |
| C. | 加强新能源研究,使用压缩天然气、氢气作汽车燃料 | |
| D. | 大量开采煤、石油及天然气以满足工业发展的需要 |
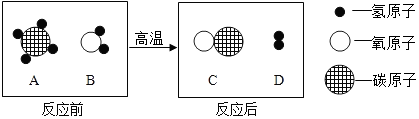
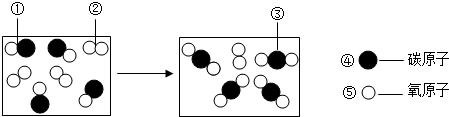

 中科院人工光合研究顶目取得重大成果:利用大自然植物叶片上含量丰富的酶作催化剂,实现了利用太阳光分解水制氢气和氧气.若分解制得的氢气和氧气的总质量为90g,则发生分解反应的水的质量为90g.
中科院人工光合研究顶目取得重大成果:利用大自然植物叶片上含量丰富的酶作催化剂,实现了利用太阳光分解水制氢气和氧气.若分解制得的氢气和氧气的总质量为90g,则发生分解反应的水的质量为90g.