题目内容
20.臭氧水是臭氧(O3)溶入水中制成的,能脱色去臭,还是很好的杀虫、杀菌剂.下列说法正确的是( )| A. | 臭氧中氧元素化合价为-2价 | B. | 臭氧是氧化物 | ||
| C. | 臭氧水是单质 | D. | 1个臭氧分子由3个氧原子构成 |
分析 A.根据单质中元素的化合价来分析;
B.根据氧化物的概念来分析;
C.根据物质的组成来分析;
D.根据分子结构来分析.
解答 解:A.臭氧是一种单质,氧元素的化合价为0,故错误;
B.臭氧是一种单质,不属于氧化物,故错误;
C.臭氧水是臭氧(O3)溶入水中制成的,属于混合物,故错误;
D.由臭氧(O3)化学式可知,1个臭氧分子由3个氧原子构成,故正确.
故选D.
点评 本题考查学生对化合价原则、单质和氧化物的概念等知识的熟悉情况,可依据已有的知识进行解答.

练习册系列答案
相关题目
6.下列判断正确的是( )
| A. | 需要加热才能发生的变化是化学变化 | |
| B. | 凡有发光、发热现象的变化都是化学变化 | |
| C. | 当两种物质相遇后,有沉淀生成,说明它们发生化学变化 | |
| D. | 生成新物质的变化一定是化学变化 |
11.完成下列化学用语题:
(1)写出下列物质的化学式:
氯气Cl2,硫酸钾K2SO4,氯化亚铁FeCl2,氧化铝Al2O3.
(2)小保同学在一次作业中出现如下几个错误:
①二个氢原子(H2); ②锌离子( Zn ); ③银元素(Hg); ④氧化铁(FeO).
请你任选其中的两个错误帮他改正过来:2H;Zn2+
(3)根据下表信息,完成表中空格:
(1)写出下列物质的化学式:
氯气Cl2,硫酸钾K2SO4,氯化亚铁FeCl2,氧化铝Al2O3.
(2)小保同学在一次作业中出现如下几个错误:
①二个氢原子(H2); ②锌离子( Zn ); ③银元素(Hg); ④氧化铁(FeO).
请你任选其中的两个错误帮他改正过来:2H;Zn2+
(3)根据下表信息,完成表中空格:
| 化学符号 | 4N2 | |||
| 符号的意义 | 三个氢原子 | 4个氮分子 | 二个铝离子 | 五氧化二磷中磷元素的化合价为+5价 |
15.实验室开放日,小红同学做了镁条在空气中燃烧的实验,发现产物中除了有大量白色固体外,还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】
①镁与氧气反应发出耀眼白光,放出热量,冒大量白烟;
②镁能与氮气在点燃的条件下剧烈反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想(请填写下列表格)
【反思与交流】
①小红通过查阅资料知道镁条还可以与氮气反应,请你帮助小红同学写出此反应的化学方程式:3Mg+N2 $\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
②空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释:因为氧气的化学性质比氮气活泼.
③小红同学对镁条燃烧实验中各物质的质量进行了研究,反应前称得镁条的质量为M1,燃烧后所产生的白色固体氧化镁的质量为M2(忽略镁条与氮气反应的影响).小红同学根据质量守恒定律,推测M1一定要小于M2,但是,称量后比较的实际结果是M1反而大于M2,请你帮助他分析其可能的原因是:镁燃烧生成的氧化镁有一部分以白烟的形式,逸散到空气中去了.
【提出问题】黄色固体是什么呢?
【查阅资料】
①镁与氧气反应发出耀眼白光,放出热量,冒大量白烟;
②镁能与氮气在点燃的条件下剧烈反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想(请填写下列表格)
| 实验操作 | 实验现象及结论 |
| 取少量黄色粉末放入试管中,加入适量水,然后将湿润的红色石蕊试纸伸入试管内,观察现象 | 若试纸变蓝,则黄色固体是Mg3N2 |
①小红通过查阅资料知道镁条还可以与氮气反应,请你帮助小红同学写出此反应的化学方程式:3Mg+N2 $\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
②空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释:因为氧气的化学性质比氮气活泼.
③小红同学对镁条燃烧实验中各物质的质量进行了研究,反应前称得镁条的质量为M1,燃烧后所产生的白色固体氧化镁的质量为M2(忽略镁条与氮气反应的影响).小红同学根据质量守恒定律,推测M1一定要小于M2,但是,称量后比较的实际结果是M1反而大于M2,请你帮助他分析其可能的原因是:镁燃烧生成的氧化镁有一部分以白烟的形式,逸散到空气中去了.
5.分类法在科学研究中具有广泛的应用.下列说法正确的是( )
| A. | 铝、银均属于金属单质,它们都能与稀硫酸反应 | |
| B. | 金刚石和石墨都是由碳元素组成的单质,它们的原子排列方式相同 | |
| C. | 盐酸、硫酸均属于酸,它们都能使紫色石蕊试液变红 | |
| D. | 一氧化碳、三氧化硫均属于非金属氧化物,它们都能与氢氧化钠溶液反应 |
12.下列说法错误的是( )
| A. | 构成物质的微粒有原子、分子、离子 | |
| B. | 墙内开花墙外香,说明分子是不断运动的 | |
| C. | 在发生化学变化时,原子种类不变,元素种类也不变 | |
| D. | 保持水的化学性质的粒子是氢分子和氧原子 |
9. 如表是元素周期表中部分元素的信息,请回答下列问题:
如表是元素周期表中部分元素的信息,请回答下列问题:
(1)氧元素的相对原子质量是16.00,氯元素的化学性质与表中氟元素(填元素符号)的化学性质相似;
(2)写出由12、17号两种元素组成的化合物的化学式MgCl2;
(3)请画出16号元素的原子结构示意图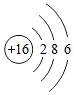 ,该元素的原子在化学反应中易得到(填“得到”或“失去”)电子;
,该元素的原子在化学反应中易得到(填“得到”或“失去”)电子;
(4)14号元素属于非金属(填“金属”或“非金属”)元素,表中不同元素最本质的区别是B(选填序号:A.相对原子质量不同 B.质子数不同 C.中子数不同).
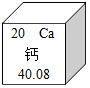
(5)如图是元素周期表中的一格,从中获取的信息错误的是D
A.该元素的原子序数为20 B.该元素属于金属元素
C.该元素的原子核外有20个电子 D.该元素的相对原子质量为40.08克.
 如表是元素周期表中部分元素的信息,请回答下列问题:
如表是元素周期表中部分元素的信息,请回答下列问题:| 第2周期 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 第3周期 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.02 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)写出由12、17号两种元素组成的化合物的化学式MgCl2;
(3)请画出16号元素的原子结构示意图
 ,该元素的原子在化学反应中易得到(填“得到”或“失去”)电子;
,该元素的原子在化学反应中易得到(填“得到”或“失去”)电子;(4)14号元素属于非金属(填“金属”或“非金属”)元素,表中不同元素最本质的区别是B(选填序号:A.相对原子质量不同 B.质子数不同 C.中子数不同).
(5)如图是元素周期表中的一格,从中获取的信息错误的是D
A.该元素的原子序数为20 B.该元素属于金属元素
C.该元素的原子核外有20个电子 D.该元素的相对原子质量为40.08克.
10.下列物质中,属于混合物的是( )
| A. | 氯酸钾 | B. | 海水 | C. | 氢气 | D. | 蒸馏水 |