题目内容
17.“碧螺春”茶叶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46.下列说法错误的是( )| A. | 单宁酸由碳、氢、氧三种元素组成 | |
| B. | 一个单宁酸分子是由76个碳原子、52个氢原子和46个氧原子构成 | |
| C. | 单宁酸中碳、氧元素的质量比为38:23 | |
| D. | 单宁酸中氢元素的质量分数最小 |
分析 A、根据单宁酸化学式的含义进行分析判断.
B、根据1个单宁酸分子的构成进行分析判断.
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
D、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答 解:A、单宁酸是由碳、氢、氧三种元素组成的,故选项说法正确.
B、一个单宁酸分子是由76个碳原子、52个氢原子和46个氧原子构成,故选项说法正确.
C、单宁酸分子中碳、氧元素的质量比为(12×76):(16×46)≠38:23,故选项说法错误.
D、单宁酸分子中C、H、O三种元素的质量比为(12×76):(1×52):(16×46)=228:13:184,则单宁酸中氢元素的质量分数最小,故选项说法正确.
故选:C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
7.下列说法中,不正确的是( )
| A. | 人类向空气中排放的一些有害物质使臭氧层受到不同程度的破坏,我国正倡导生产和使用无氟冰箱 | |
| B. | 无铅汽油的使用可以提高城乡空气质量 | |
| C. | 保护森林植被,大规模进行人工造林和绿化,是防止空气污染的重要措施 | |
| D. | 稀有气体很难和其他物质发生反应,所以没有多大用途 |
12.下列物质的用途中,利用其化学性质的是( )
| A. | 干冰用于人工降雨 | B. | 稀有气体用作多用途的电光源 | ||
| C. | 焊接金属时用氮气作保护气 | D. | 铜用于制作导线 |
6.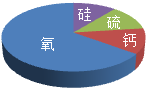 某陨石中含有如图所示的四种元素,该陨石中可能含有的物质是( )
某陨石中含有如图所示的四种元素,该陨石中可能含有的物质是( )
 某陨石中含有如图所示的四种元素,该陨石中可能含有的物质是( )
某陨石中含有如图所示的四种元素,该陨石中可能含有的物质是( )| A. | CaCl2 | B. | SiO2 | C. | CaCO3 | D. | Fe2O3 |
7.废铁屑的主要成份是铁,同时还有少量铁锈(Fe2O3),动物饲料硫酸亚铁的生产工艺之一如图所示:
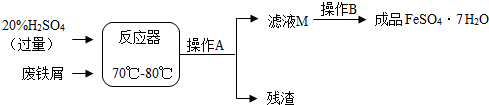
(1)在反应器中发生反应的化学方程式除Fe2(SO4)3+Fe═3FeSO4外,写出发生的其他一个化学反应方程式:Fe+H2SO4=FeSO4+H2↑、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(2)在实验室中操作A是过滤;
(3)滤液M经过操作B可得硫酸亚铁晶体(FeSO4•7H2O).已知硫酸亚铁的溶解度和析出晶体的组成如下表:
根据溶解度表,要得到纯净的硫酸亚铁晶体(FeSO4•7H2O),冷却结晶温度应该低于
64℃;待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次.用冰水洗涤的目的是:
Ⅰ除去晶体表面附着的杂质;Ⅱ减少晶体溶解,提高产率.
(4)在化学反应中,将有元素化合价变化的反应定义为氧化还原反应.在氧化还原反应中,若有元素的化合价升高,必有元素的化合价降低,且元素化合价升降总数相等.将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它氧化物,试写出该氧化还原反应的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3.

(1)在反应器中发生反应的化学方程式除Fe2(SO4)3+Fe═3FeSO4外,写出发生的其他一个化学反应方程式:Fe+H2SO4=FeSO4+H2↑、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(2)在实验室中操作A是过滤;
(3)滤液M经过操作B可得硫酸亚铁晶体(FeSO4•7H2O).已知硫酸亚铁的溶解度和析出晶体的组成如下表:
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | ||
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | ||
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||||
64℃;待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次.用冰水洗涤的目的是:
Ⅰ除去晶体表面附着的杂质;Ⅱ减少晶体溶解,提高产率.
(4)在化学反应中,将有元素化合价变化的反应定义为氧化还原反应.在氧化还原反应中,若有元素的化合价升高,必有元素的化合价降低,且元素化合价升降总数相等.将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它氧化物,试写出该氧化还原反应的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3.
