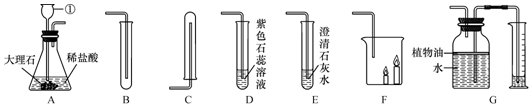
题目内容
8.当二氧化碳气体通入氢氧化钠溶液时观察不到明显的现象,请你设计一个实验证明两者确实是发生了反应.分析 根据二氧化碳和氢氧化钠反应生成碳酸钠和水;碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳进行分析.
解答 解:由于二氧化碳气体通入氢氧化钠溶液时观察不到明显的现象,并且二氧化碳能够溶于水,可以根据二氧化碳和氢氧化钠反应生成碳酸钠和水;碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳气体设计实验,所以取混合后的溶液于试管中,加入足量稀盐酸,产生气泡,说明氢氧化钠和二氧化碳发生了反应.
故答案为:取混合后的溶液于试管中,加入足量稀盐酸,产生气泡,说明氢氧化钠和二氧化碳发生了反应.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
19.将溶质的质量分数为30%的硫酸溶液100克与溶质的质量分数为50%的硫酸溶液100克混合,混合溶液的溶质的质量分数为( )
| A. | 80% | B. | 40% | C. | 15% | D. | 25% |
16.有A、B两种混合粉末,质量分别为m1,m2.A由CaCO3和KHCO3组成,B由MgCO3和NaHCO3组成.将A、B分别与足量稀盐酸反应,生成二氧化碳气体的质量均为wg.下列说法正确的是( )
(已知:KHCO3+HCl=KCl+CO2↑+H2O,NaHCO3+HCl=NaCl+CO2↑+H2O )
(已知:KHCO3+HCl=KCl+CO2↑+H2O,NaHCO3+HCl=NaCl+CO2↑+H2O )
| A. | m1=m2 | |
| B. | 混合物A中CaCO3和KHCO3质量比一定为1:1 | |
| C. | 21ml=25m2 | |
| D. | 混合物B中MgCO3和NaHCO3质量比一定为1:1 |
13.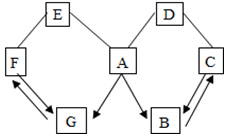 如图所示A~G是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知A是人体胃液中含有的酸,G是最轻的气体,B、C、D、E、F都是氧化物.下列说法不正确的是( )
如图所示A~G是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知A是人体胃液中含有的酸,G是最轻的气体,B、C、D、E、F都是氧化物.下列说法不正确的是( )
 如图所示A~G是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知A是人体胃液中含有的酸,G是最轻的气体,B、C、D、E、F都是氧化物.下列说法不正确的是( )
如图所示A~G是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知A是人体胃液中含有的酸,G是最轻的气体,B、C、D、E、F都是氧化物.下列说法不正确的是( )| A. | 整个过程可能涉及4种反应类型 | B. | E与F的反应是放热反应 | ||
| C. | B和C一定含有相同的元素 | D. | C和D发生的反应可能是置换反应 |
17.用下图操作可完成甲、乙两个实验.甲实验为配制溶质的质量分数为20%的氯化钠溶液25克,乙实验为粗盐中难溶性杂质的去除.下列说法中,正确的是( )
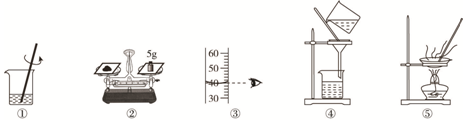

| A. | 甲实验按照③②①的步骤,如图所示操作,配制的溶液浓度偏小 | |
| B. | 操作②中,若将食盐和砝码互换位置,配制的溶液浓度偏小 | |
| C. | 各步骤作中的玻璃棒都是用来搅拌 | |
| D. | 乙实验步骤是①④⑤,其中⑤当蒸发皿出现较多固体时,就应停止加热 |
18.下列生活用品中,用金属材料制作的是( )
| A. |  瓷器 瓷器 | B. |  铁罐 | C. |  铅笔 铅笔 | D. |  塑料杯 |
 世园会植物馆号称亚洲第一大钢结构管,拼装钢材杆件达到14000多根,所有杆件均为现场拼装焊接.
世园会植物馆号称亚洲第一大钢结构管,拼装钢材杆件达到14000多根,所有杆件均为现场拼装焊接.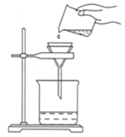 2016年我省某市初中化学实验操作技能考察中,小强同学抽到的试题是“水的净化”,请你与小强一起实验,并回答下列问题.
2016年我省某市初中化学实验操作技能考察中,小强同学抽到的试题是“水的净化”,请你与小强一起实验,并回答下列问题.