题目内容
8.在一只密闭容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表:| 物质 | X | Y | Z | Q |
| 反应前质量/g | 8 | 2 | 40 | 5 |
| 反应后质量/g | 待测 | 24 | 8 | 23 |
A.其中X、Z为反应物 B.反应后生成Y、Q的质量比为24:23
C.反应后X的质量为0 D.其中X、Z为生成物.
分析 根据质量守恒定律可得出反应后A的质量,然后分析各物质在反应前后的变化量可得出反应物和生成物,质量减少的是反应物,质量增加的是生成物;化合反应是“多变一”的反应.
解答 解:A、根据质量守恒定律,反应后物质X的质量为:(8+2+40+5)g-(24+8+23)g=0g,X、Z的质量减少,所以X、Z是反应物,故A正确;
B、反应后生成Y、Q的质量比为22g:18g=11:9,故B错误;
C、根据质量守恒定律,反应后物质X的质量为:(8+2+40+5)g-(24+8+23)g=0g,故C正确;
D、通过分析可知,X、Z是反应物,Y、Q是生成物,故D错误.
故答案为:B,其中X、Z为生成物.
点评 本题主要考查了质量守恒定律的应用和化合反应、分解反应、置换反应、氧化反应的分辨,难度不大.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
19.下列方程式书写正确的是( )
| A. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ | B. | Mg+O2═2MgO2↑ | ||
| C. | 4Fe+3O2$\frac{\underline{\;高温\;}}{\;}$2FeO3 | D. | C+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2↑ |
16.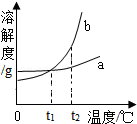 如图是a、b两种固体物质(不含结晶水)的溶解度曲线.下列说法正确的是
如图是a、b两种固体物质(不含结晶水)的溶解度曲线.下列说法正确的是
( )
 如图是a、b两种固体物质(不含结晶水)的溶解度曲线.下列说法正确的是
如图是a、b两种固体物质(不含结晶水)的溶解度曲线.下列说法正确的是( )
| A. | t2℃时,a溶液的溶质质量分数一定小于b溶液的溶质质量分数 | |
| B. | t1℃时,将a、b两种物质的饱和溶液分别恒温蒸发等质量的水, 析出晶体的质量一定相等 | |
| C. | 将t2℃时b的不饱和溶液降温至t1℃,一定能得到b的饱和溶液 | |
| D. | 若a中混有少量的b,可以降温结晶的方法提纯a |
3.“高效环保芳烃成套技术开发及应用”项目荣获了2015年度国家科学技术进步特等奖.芳烃成套技术以生产对二甲苯为核心,是一个国家石油化工发展水平的标志性技术之一.二甲苯的化学式为C6H4(CH3)2,下列说法正确的是( )
| A. | .二甲苯是由8个碳原子、10个氢原子构成 | |
| B. | .C6H4(CH3)2中C、H原子的个数比为4:5 | |
| C. | .二甲苯的相对分子质量是106g | |
| D. | .二甲苯中碳元素与氢元素的质量比为8:10 |
17.从分子的角度分析,下列解释错误的是( )
| A. | 液氧和氧气都能助燃----同种分子的化学性质相同 | |
| B. | 气体受热膨胀----温度升高,气体分子体积变大 | |
| C. | 新装修的房间常有刺激性气味----分子在不断地运动 | |
| D. | 水电解生成氢气和氧气----分子拆成原子,原子重新结合成分子 |
18.推理是化学学习中常用的思维方法.下列推理正确的是( )
| A. | 化合物是含有不同元素的纯净物,则含有不同种元素的纯净物一定是化合物 | |
| B. | 铝表面的氧化铝薄膜能起到保护作用,则铁表面的氧化铁也能起到保护作用 | |
| C. | 浓硫酸具有吸水性,则浓盐酸也具有吸水性 | |
| D. | 分子、原子可以构成物质,则物质一定都是由分子、原子构成的 |
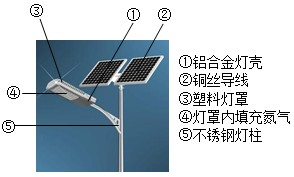 随着科技的不断进步,太阳能路灯(如图所示)越来越多的出现在我们城市道路的两旁. 节约能源的同时减少了环境的污染,是实现“低碳生活”的一种典型措施.请你根据图中内容回答下列问题:
随着科技的不断进步,太阳能路灯(如图所示)越来越多的出现在我们城市道路的两旁. 节约能源的同时减少了环境的污染,是实现“低碳生活”的一种典型措施.请你根据图中内容回答下列问题: