题目内容
17. N(NO2)2是科学家2011年发现的一种新型火箭燃料,试计算:
N(NO2)2是科学家2011年发现的一种新型火箭燃料,试计算:(1)N(NO2)2是由2种元素组成的,其相对分子质量为106.
(2)N(NO2)2中氮元素的质量分数为39.6%.(结果保留一位小数)
(3)①U形管中是滴有酚酞试液的蒸馏水,向左、右两管中分别同时滴加20g氢氧化钠溶液和20g稀盐酸(如图所示),下列说法正确的是
A、开始时左边溶液呈红色,右边溶液呈无色
B、开始时左边溶液呈无色,右边溶液呈红色
C、充分反应后U形管中的溶液呈中性
D、充分反应后U形管中的溶液呈无色
②用20g15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,洗涤后的溶液呈中性,这一定量石油产品中含H2SO4的质量是多少?石油产品中含H2SO4的质量是3.675g.
分析 (1)根据化学式可知物质的元素组成,相对分子质量=各原子的相对原子质量×原子个数之和,进行分析解答;
(2)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答;
(3)①酚酞试液在碱性溶液中为红色,在酸性和中性溶液中为无色,不知氢氧化钠溶液和稀盐酸的溶质质量分数,无法判断反应后溶液的酸碱性;
②据氢氧化钠溶液的质量和溶质质量分数可知溶液中氢氧化钠的质量,并结合方程式计算出硫酸的质量.
解答 解:(1)由N(NO2)3可知该物质由氮元素和氧元素两种元素组成;
其相对分子质量=14+(14+16×2)×2=106;
(2)N(NO2)2中氮元素的质量分数为$\frac{14×3}{106}$×100%≈39.6%;
(3)①A、左管加入的是氢氧化钠溶液,开始时显红色,右管加入的是盐酸,开始时显示无色,故A正确;
B、由A分析可知:左管开始时显红色,右管开始时显示无色,故B错误;
C、不知道20g氢氧化钠溶液和20g稀盐酸的溶质质量分数,故无法判断二者是否恰好完全反应,从而无法判断溶液的酸碱性,故C错误;
D、由C可知无法判断最终溶液的酸碱性,故无法判断酚酞在溶液中的变色情况,故D错误;
②设石油产品中硫酸质量为x
2NaOH+H2SO4═Na2SO4+2H2O,
80 98
20g×15% x
$\frac{80}{98}$=$\frac{20g×15%}{x}$
x=3.675g
故答案为:(1)2;106;
(2)39.6%;
(3)①A;②石油产品中含H2SO4的质量是3.675g.
点评 本题考查同学们结合新信息、灵活运用化学式的有关计算,及酸和碱反应、溶液的酸碱性与酚酞试液的关系,应用化学方程式进行计算的能力,能较好考查学生进行分析问题、解决问题的能力.

| A. |  闻气体气味 | B. |  取用块状固体 | C. | 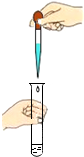 滴加液体 滴加液体 | D. | 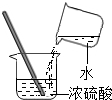 稀释浓硫酸 |
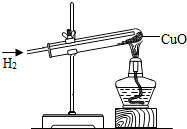 如图所示为氢气还原氧化铜,在实验中,可观察到的现象是( )
如图所示为氢气还原氧化铜,在实验中,可观察到的现象是( )| A. | 氧化铜变成红色的铜 | |
| B. | 氧化铜变成铜,同时有水生成 | |
| C. | 氧化铜变成钢,氢气被氧化为水 | |
| D. | 黑色粉末变成光亮的红色物质,试管口有水珠生成 |
| A. | 酒香不怕巷子深--微粒在不停运动 | |
| B. | Na和Na+都属于钠元素--两种微粒的电子数相同 | |
| C. | 18g水中大约有6.02×1023个水分子--分子的质量很小 | |
| D. | 食盐溶液能导电--溶液中存在能自由移动的离子 |
①反应条件是点燃 ②反应前后元素的种类不变
③反应前后分子的总数不变④参加反应的物质是磷和氧气.
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
| A. | 浓硫酸 | B. | 烧碱 | C. | 氧化钙 | D. | 硅胶 |
| 选项 | 实验目的 | 实验操作 |
| A | 鉴别硫酸钙和硫酸钡粉末 | 加水 |
| B | 鉴别氢气和甲烷 | 闻气味 |
| C | 除去氯化铜溶液中的硫酸铜 | 加适量的氯化钡溶液,充分反应后过滤 |
| D | 除去铜粉中的氧化铁粉末 | 用磁铁吸 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 燃烧不一定有氧气参加 | |
| B. | 只要有盐和水生成的反应就一定是中和反应 | |
| C. | 一种单质和一种化合物发生的反应不一定是置换反应 | |
| D. | 饱和溶液析出晶体后,剩余溶液中溶质的质量分数可能不变 |
| A. | “伊利”纯牛奶 | B. | “娃哈哈”矿泉水 | C. | 肥皂水 | D. | 血液 |