题目内容
2.炼铁的原理是利用一氧化碳和氧化铁的反应,化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.分析 炼铁的原理是利用一氧化碳和氧化铁的反应,生成铁和二氧化碳,写出反应的化学方程式即可.
解答 解:炼铁的原理是利用一氧化碳和氧化铁的反应,生成铁和二氧化碳,反应的化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
故答案为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
点评 本题难度不大,掌握工业上炼铁的原理、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12. 化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a、可能与金属本身的性质有关
b、可能与盐酸的浓度有关
【设计探究】实验所用金属均已用砂纸打磨.
实验(1)为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入相同浓度和质量的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,发生反应的化学方程式有Zn+2HCl=ZnCl2+H2↑、Fe+2HCl=FeCl2+H2↑;.从实验现象可判断:金属活动性Zn>Fe(填“<”“=”“>”).
得出结论:金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是金属活动性越强,反应的程度越剧烈.
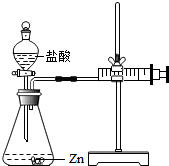
实验(2)为探究猜想b,小组同学设计如图的装置进行实验,其中注射器的作用是量取生成气体的体积.所用药品,实验数据如表:
得出结论:金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是盐酸浓度越大,反应程度越剧烈.
【反思评价】根据表一中实验Ⅱ数据分析,请描述锌与盐酸发生反应快慢的变化情况并解释原因锌与盐酸反应产生气体的速度先加快后变慢,因为锌与盐酸是放热反应,所以开始时温度升高,产生气体速度加快,随着反应的进程,盐酸不断被消耗,浓度降低,产生气体速度变慢
通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响固体的表面积.(写出一条即可)
【拓展延伸】很多金属不仅能与酸反应,也能与盐溶液反应,将铁棒放入硫酸铜溶液中,在铁棒上析出红色物质,过一段时间后,取出铁棒称量,发现质量比原来增加4g,则生成铜的质量为32g.
 化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a、可能与金属本身的性质有关
b、可能与盐酸的浓度有关
【设计探究】实验所用金属均已用砂纸打磨.
实验(1)为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入相同浓度和质量的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,发生反应的化学方程式有Zn+2HCl=ZnCl2+H2↑、Fe+2HCl=FeCl2+H2↑;.从实验现象可判断:金属活动性Zn>Fe(填“<”“=”“>”).
得出结论:金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是金属活动性越强,反应的程度越剧烈.
实验(2)为探究猜想b,小组同学设计如图的装置进行实验,其中注射器的作用是量取生成气体的体积.所用药品,实验数据如表:
| 实验编号 | 选用金属(均取2g) | 盐酸质量分数(均取50mL) | 每分钟产生氢气的体积/mL | |||||
| 1分钟 | 1-2分钟 | 2-3分钟 | 3-4分钟 | 4-5分钟 | 前5分钟共收集气体 | |||
| Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.0 | 9.2 | 7.6 | 48.5 |
| Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
【反思评价】根据表一中实验Ⅱ数据分析,请描述锌与盐酸发生反应快慢的变化情况并解释原因锌与盐酸反应产生气体的速度先加快后变慢,因为锌与盐酸是放热反应,所以开始时温度升高,产生气体速度加快,随着反应的进程,盐酸不断被消耗,浓度降低,产生气体速度变慢
通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响固体的表面积.(写出一条即可)
【拓展延伸】很多金属不仅能与酸反应,也能与盐溶液反应,将铁棒放入硫酸铜溶液中,在铁棒上析出红色物质,过一段时间后,取出铁棒称量,发现质量比原来增加4g,则生成铜的质量为32g.
5.下列物质的用途是利用其化学性质的是( )
| A. | 干冰用于人工降雨 | B. | 液氮用作制冷剂 | ||
| C. | 肥皂水用于区别硬水和软水 | D. | 氦气用作探空气球 |
12.在化学反应A+2B=2C+D中,C和D的化学式量之比为9:22,今有16克A完全反应生成44克D,则参加反应的B的质量是( )
| A. | 16g | B. | 32g | C. | 64g | D. | 44g |