题目内容
用下列装置进行证明质量守恒定律的实验,反应前后容器中物质的总质量不相等的是( )
|
| A. |
| B. |
| C. |
| D. |
|
| 质量守恒定律及其应用. | |
| 专题: | 化学用语和质量守恒定律. |
| 分析: | 在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变. |
| 解答: | 解:A、白磷燃烧能生成五氧化二磷,遵循质量守恒定律,并且装置是一个密闭系统,反应前后容器中物质的总质量相等. B、虽然容器敞口,但是氢氧化钠溶液和硫酸铜溶液反应能生成硫酸钠和氢氧化铜,不产生气体,所以反应前后容器中物质的总质量相等. C、容器敞口,石灰石中的碳酸钙和稀盐酸反应能生成氯化钙、水和二氧化碳,二氧化碳逸出,使得反应前后容器中物质的总质量不相等. D、双氧水在二氧化锰的作用下分解能生成水和氧气,虽然生成气体,但是装置是一个密闭系统,生成的氧气不能逸出密闭系统,反应前后容器中物质的总质量相等. 故选:C. |
| 点评: | 化学反应都遵循质量守恒定律,和反应前后容器中物质的总质量是否相等无关,造成质量是否相等与装置的结构有关. |

下列化学方程式书写正确的是( )
|
| A. | 氧化汞加热分解:2HgO═2Hg+O2↑ |
|
| B. | 硫在氧气中燃烧:S+O2↑ |
|
| C. | 红磷在空气中燃烧:4P+5O2 |
|
| D. | 硫酸铜溶液(CuSO4)和氢氧化钠溶液(NaOH)反应生成硫酸钠(Na2SO4)和氢氧化铜[Cu(OH)2]沉淀:CuSO4+NaOH=Na2SO4+Cu(OH)2↓ |
老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:
(1)①此气体是什么物质?验证它的实验方案如下:
| 猜 想 | 验证猜想的实验步骤 | 现象及结论 |
| 我认为此气体可 能是 O2 | . | . |
| 产生此气体的一个化学方程式是 . |
②我想制取该气体,发生装置将选取下图中的 (填序号,以下同),收集装置选取 .
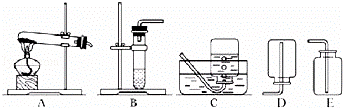
(2)我猜想无色气体还可能是另外一种气体,产生它的其中一个化学方程式是: .
(3)晴晴同学为测定某石灰石中碳酸钙的质量分数(杂质不与酸反应),向6.0g石灰石样品中逐滴加入稀盐酸至不再产生气泡为止,共生成二氧化碳气体2.2g.试计算:该石灰石样品中碳酸钙的质量分数.
在天平两盘的烧杯中,各放入质量相同的稀盐酸,调节天平至平衡,分别向两边烧杯中各加入5g镁和5g铁,镁和铁全部反应而消失后,天平的指针( )
|
| A. | 偏向加铁的一边 |
|
| B. | 偏向加镁的一边 |
|
| C. | 先偏向加镁的一边,后偏向加铁的一边 |
|
| D. | 最终仍停留在原来的位置 |
下列有关资源的叙述正确的是( )
|
| A. | 矿物的储量有限,有些可以再生 |
|
| B. | 海洋是地球上巨大的资源宝库,海水中含80多种物质 |
|
| C. | 氯化钠在自然界分布很广,工业上可以氯化钠为原料制取氢氧化钠 |
|
| D. | 废旧金属可回收再利用,但不包括被腐蚀的铁制品 |




 SO2
SO2 2P2O5
2P2O5 %的磁铁矿石,理论上冶炼含杂质4%的生铁多少吨?(答案保留一位小数)
%的磁铁矿石,理论上冶炼含杂质4%的生铁多少吨?(答案保留一位小数)