题目内容
9. 如图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述正确的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述正确的是( )| A. | t1℃时,等质量的甲、乙溶液中所含溶质的质量为乙>甲 | |
| B. | t2℃时,20g丙能溶解于50g水中形成70g溶液 | |
| C. | 若要将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法 | |
| D. | t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液溶质质量分数的大小关系为乙>甲>丙 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、要比较某一温度下两种溶液中溶质的质量分数,必须等质量的饱和溶液,本题没有说明是饱和溶液,无法比较,故错误;
B、t2℃时,丙的溶解度为30g,20g丙溶解于50g水中,有5g丙未溶解,能形成65g溶液,故错误;
C、物质的溶解度随温度的升高而增大,所以要将组成在N点的甲溶液转变为M点的甲溶液,可以采用恒温蒸发溶剂或添加溶质的方法,故正确;
D、甲、乙的溶解度随温度的降低而减小,丙的溶解度随温度的降低而增大,所以将t3℃时甲、乙、丙的饱和溶液降温到t2℃,甲乙析出晶体,依然为饱和溶液,丙变为不饱和溶液,溶质质量分数与降温前相等,由饱和溶液中溶质质量分数的计算式$\frac{溶解度}{100g+溶解度}$×100%可知,溶解度越大质量分数也就越大,t2℃时乙的溶解度大于甲,且t2℃时甲的溶解度大于t3℃时丙的溶解度,所以此时溶液的质量分数由大到小的顺序为乙>甲>丙,故正确;
故选:CD.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
19.向5.6g铁中加入200g硫酸溶液,铁与硫酸恰好完全反应,下列有关说法正确的是( )
| A. | 反应后溶液中的溶质是Fe2(SO4)3 | B. | 反应后溶液中SO42-质量是9.8g | ||
| C. | 原硫酸溶液的溶质质量分数是4.9% | D. | 反应后溶液的质量是205.5g |
4.下列有关水和溶液的说法正确的是( )
| A. | 河水经过沉降、过滤、活性炭吸附后得到的水是纯净物 | |
| B. | 饱和溶液析出晶体后,溶液的溶质质量分数不一定减少 | |
| C. | 通过洗洁精的乳化作用,可将食用油溶解于水形成溶液 | |
| D. | 试剂瓶中的溶液在使用时不慎洒出一部分,剩余溶液溶质质量分数减少 |
17.为了书写和学术交流的方便,常采用国际统一的符号.下列符号中表示2个氮原子的是( )
| A. | 2N | B. | N2 | C. | 2 N2 | D. | 2Na |
18.下列成语中一定包含化学变化的是( )
| A. | 铁杵成针 | B. | 破釜沉舟 | C. | 百炼成钢 | D. | 水到渠成 |
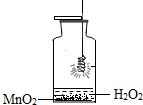 如图所示是铁丝在氧气中燃烧的改进实验,用适量双氧水和二氧化锰代替原实验中集气瓶里的水.
如图所示是铁丝在氧气中燃烧的改进实验,用适量双氧水和二氧化锰代替原实验中集气瓶里的水.