题目内容
19.以下四组离子,能大量共存且能形成无色透明溶液的是( )| A. | Fe3+Ag+ Cl- SO42- | B. | Mg2+Cu2+Cl- OH- | ||
| C. | H+ Na+ K+ NO3- | D. | H+ Ba2+NO3- SO42- |
分析 根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能共存;本题还要注意溶液呈无色透明,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:A、四种离子间不能结合成沉淀、气体或水,能大量共存;但Fe3+的水溶液黄色,故选项错误;
B、Mg2+与OH-能结合成氢氧化镁白色沉淀,Cu2+与OH-能结合成氢氧化铜蓝色,不能大量共存,故选项错误;
C、四种离子间不能结合成沉淀、气体或水,能大量共存;且不存在有色离子,故选项正确;
D、Ba2+与SO42-能结合成硫酸钡白色沉淀,不能大量共存,故选项错误;
故选:C.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水;溶液是无色时,不能有带色的离子.

练习册系列答案
相关题目
10.下列图象分别与操作相对应,其中合理的是( )
| A. | 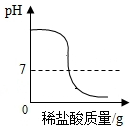 向一定量氢氧化钠溶液中滴加稀盐酸 | |
| B. | 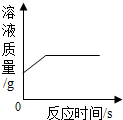 向一定量硝酸银溶液中加入一定量锌 | |
| C. | 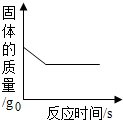 向一定量二氧化锰固体中加入一定量过氧化氢溶液 | |
| D. | 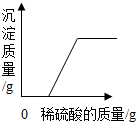 向一定量氢氧化钠和氯化钡的混合溶液中滴加稀硫酸 |
14.下列化学符号中的数字表示的意义不正确的是( )
| A. | 2Na:“2”表示两个钠元素 | |
| B. | NO2:“2”表示一个二氧化氮分子含有两个氧原子 | |
| C. | $\stackrel{+2}{Mg}O$:“+2”表示氧化镁中镁元素的化合价为+2价 | |
| D. | 2OH-:“2”表示两个氢氧根离子 |
4.小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁.铜的活动性强弱,遨请你一同参与.
【知识回放】金属活动性顺序:K Ca Na Mg Al ZnFe Sn Pb(H) Hg Ag Pt Au.请你在横线上填写对应金属的元素符号.
【做出猜想】猜想l:Cr>Fe>Cu;猜想2:Fe>Cu>Cr;猜想 3:你的猜想是Fe>Cr>Cu.
【査阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜
(2)铬能与稀硫酸反应.生成蓝色的硫酸亚铬(CrSO4)溶液
【设计与实验】小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
【结论与解择】
(1)小聪得到的结论是猜想1正确.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【知识运用】将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式Cr+FeSO4=Fe+CrSO4.
【知识回放】金属活动性顺序:K Ca Na Mg Al ZnFe Sn Pb(H) Hg Ag Pt Au.请你在横线上填写对应金属的元素符号.
【做出猜想】猜想l:Cr>Fe>Cu;猜想2:Fe>Cu>Cr;猜想 3:你的猜想是Fe>Cr>Cu.
【査阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜
(2)铬能与稀硫酸反应.生成蓝色的硫酸亚铬(CrSO4)溶液
【设计与实验】小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验操作 | 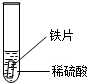 | 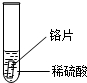 | 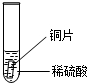 |
| 实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变为蓝色 | 无明显现象发生 |
(1)小聪得到的结论是猜想1正确.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【知识运用】将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式Cr+FeSO4=Fe+CrSO4.
8.正确操作是实验成功的保证.下列图示中,操作错误的是( )
| A. | 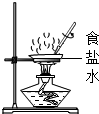 蒸发食盐水 | B. | 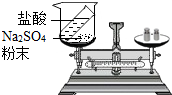 验证质量守恒定律 | ||
| C. | 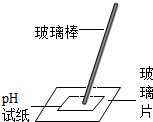 测定溶液的pH值 | D. | 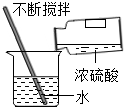 稀释浓硫酸 |

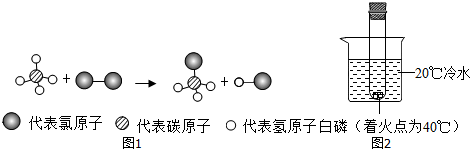
 ”表示一个氮原子,则“
”表示一个氮原子,则“ ”表示N2(填化学符号).
”表示N2(填化学符号).