题目内容
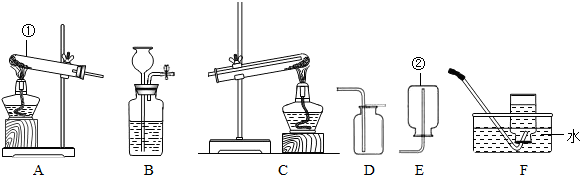
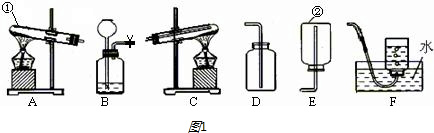
某同学用如图装置制氧气,请问答:(提示:浓硫酸具有吸水性)
(1)用高锰酸钾制取和收集氧气的装置应选用
(2)检查装置②气密性的方法是
(3)装置②试管口要略向下倾斜的原因是
④停止加热时,先要
(4)若用装置④收集的氧气不纯,其原因可能是(请写两种原因):①
(5)若要制得干燥、纯净的氧气则需要的一套装置是(填序号)
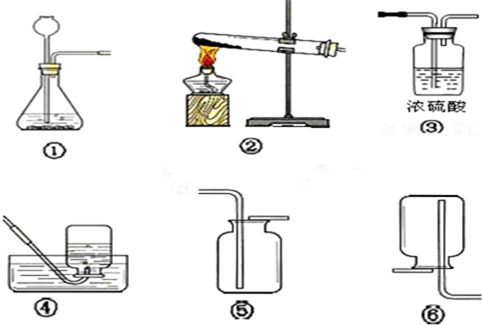
(1)用高锰酸钾制取和收集氧气的装置应选用
②④或②⑤
②④或②⑤
填序号);写出该反应的文字表达式:高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
(2)检查装置②气密性的方法是
把导气管放入水中,用双手握住试管的外壁,看到导管口有气泡冒出或松开双手,导管口形成一段水柱,说明气密性良好
把导气管放入水中,用双手握住试管的外壁,看到导管口有气泡冒出或松开双手,导管口形成一段水柱,说明气密性良好
;(3)装置②试管口要略向下倾斜的原因是
防止冷凝水倒流引起试管的炸裂
防止冷凝水倒流引起试管的炸裂
;④停止加热时,先要
将导管移出水面
将导管移出水面
,然后再熄灭酒精灯
再熄灭酒精灯
.目的是为防止熄灭酒精灯后试管骤冷,导致水沿导气管倒流引起试管的炸裂
为防止熄灭酒精灯后试管骤冷,导致水沿导气管倒流引起试管的炸裂
(4)若用装置④收集的氧气不纯,其原因可能是(请写两种原因):①
集气瓶中没装满水留有气泡
集气瓶中没装满水留有气泡
;②没等气泡连续均匀冒出时就收集氧气
没等气泡连续均匀冒出时就收集氧气
(5)若要制得干燥、纯净的氧气则需要的一套装置是(填序号)
②③⑤
②③⑤

分析:(1)根据反应物的状态和反应条件选择发生装置,根据气体的密度选择收集装置;
(2)利用加热法产生的现象判断简易装置的气密性;
(3)根据给试管中的固体加热时的注意事项分析;根据制取氧气的注意事项分析;
(4)用排水法收集氧气不纯是操作上的原因,导致混入空气;
(5)浓硫酸具有吸水性,可以用来干燥氧气,用排空气法收集.
(2)利用加热法产生的现象判断简易装置的气密性;
(3)根据给试管中的固体加热时的注意事项分析;根据制取氧气的注意事项分析;
(4)用排水法收集氧气不纯是操作上的原因,导致混入空气;
(5)浓硫酸具有吸水性,可以用来干燥氧气,用排空气法收集.
解答:解:(1)实验室用高锰酸钾制取氧气时,属于固体加热型,故选择的发生装置是②;因为氧气不易溶于水,密度比空气大,故可以采用排水法④或向上排空气法⑤收集;反应的文字表达式为:高锰酸钾
锰酸钾+二氧化锰+氧气;
(2)检查装置②气密性的方法是:把导气管放入水中,用双手握住试管的外壁,看到导管口有气泡冒出或松开双手,导管口形成一段水柱,说明气密性良好;
(3)给试管中的固体加热时试管口要略向下倾斜的原因是:防止冷凝水倒流引起试管的炸裂;
用排水法收集满气体后,为防止熄灭酒精灯后试管骤冷,导致水沿导气管倒流引起试管的炸裂,要先将导管移出水面,然后熄灭酒精灯;
(4)用排水法收集的气体不纯的可能原因有:集气瓶中没装满水留有气泡或没等气泡连续均匀冒出时就收集氧气;
(5)若要制得干燥、纯净的氧气,需要浓硫酸干燥,用向上排空气法收集,所以选择的发生装置、干燥装置、收集装置为:②③⑤.
故答案为:(1)②④或②⑤;高锰酸钾
锰酸钾+二氧化锰+氧气;
(2)把导气管放入水中,用双手握住试管的外壁,看到导管口有气泡冒出或松开双手,导管口形成一段水柱,说明气密性良好;
(3)防止冷凝水倒流引起试管的炸裂;将导管移出水面;再熄灭酒精灯;为防止熄灭酒精灯后试管骤冷,导致水沿导气管倒流引起试管的炸裂;
(4)集气瓶中没装满水留有气泡或没等气泡连续均匀冒出时就收集氧气;
(5)②③⑤
| 加热 |
(2)检查装置②气密性的方法是:把导气管放入水中,用双手握住试管的外壁,看到导管口有气泡冒出或松开双手,导管口形成一段水柱,说明气密性良好;
(3)给试管中的固体加热时试管口要略向下倾斜的原因是:防止冷凝水倒流引起试管的炸裂;
用排水法收集满气体后,为防止熄灭酒精灯后试管骤冷,导致水沿导气管倒流引起试管的炸裂,要先将导管移出水面,然后熄灭酒精灯;
(4)用排水法收集的气体不纯的可能原因有:集气瓶中没装满水留有气泡或没等气泡连续均匀冒出时就收集氧气;
(5)若要制得干燥、纯净的氧气,需要浓硫酸干燥,用向上排空气法收集,所以选择的发生装置、干燥装置、收集装置为:②③⑤.
故答案为:(1)②④或②⑤;高锰酸钾
| 加热 |
(2)把导气管放入水中,用双手握住试管的外壁,看到导管口有气泡冒出或松开双手,导管口形成一段水柱,说明气密性良好;
(3)防止冷凝水倒流引起试管的炸裂;将导管移出水面;再熄灭酒精灯;为防止熄灭酒精灯后试管骤冷,导致水沿导气管倒流引起试管的炸裂;
(4)集气瓶中没装满水留有气泡或没等气泡连续均匀冒出时就收集氧气;
(5)②③⑤
点评:本题考查了气体的制取,装置气密性的检查及实验注意事项,属于基础知识的考查,关键是平时扎实基础的学习,并能够灵活运用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.
提出问题 这种淡黄色粉末是什么?有什么性质和用途?
查阅资料 ①硫是淡黄色粉末,不溶于水;
②过氧化钠(Na2O2)是淡黄色粉末,溶于水并能与水反应,“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”
猜想与探究
猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物.
实验与结论
| 实验操作 | 实验现象 | 实验结论 | |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水,充分振荡 | ________ | 猜想a、c不成立,猜想b成立. |
提出猜想 过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气.
进行实验
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气. 王轩同学设计如图Ⅰ所示装置:

(1)实验现象及结论:观察到________现象,判断过氧化钠与氮气没有发生反应.
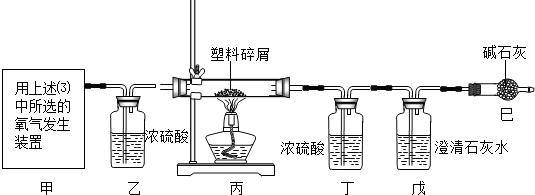
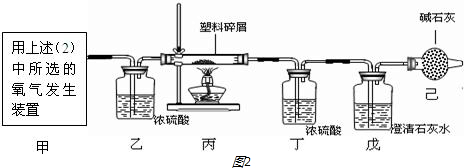
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气. 华宇同学设计了如下图所示装置
(2)其中A装置的作用是________.
(3)实验现象及结论:带火星的木条复燃;查阅资料知道:过氧化钠与水蒸气生成了氧气和一种常见碱,写出该反应的化学方程式________.
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气.
李杰在老师的指导下也设计了如图Ⅱ所示装置.(不考虑稀盐酸的挥发)
(4)实验记录
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. | 装置的气密性良好. | |
| ② | 打开分液漏斗活塞,向A 装置中缓慢加入稀盐酸. | A装置中观察到的现象有________, C装置中有气泡出现. | A装置中发生反应的化学方程式为________; C装置作用是________. |
| ③ | 一段时间后用带火星的木条在D内进行检验. | 带火星的木条复燃. | 过氧化钠与二氧化碳反应并生成氧气. |
(1)张红同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是________.请你回答如何改进该实验________.
(2)王兵同学查阅资料后知道实验Ⅲ中过氧化钠与二氧化碳反应生成碳酸钠和氧气,他称取过氧化钠与二氧化碳充分反应后的固体剩余物质21.5g,加入到盛有足量稀盐酸的烧杯中,并不断用玻璃棒搅拌.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图Ⅳ所示(不考虑实验过程中其它因素的影响).
请计算碳酸钠的质量分数:________.(写出计算过程,结果保留一位小数)

某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.
提出问题 这种淡黄色粉末是什么?有什么性质和用途?
查阅资料 ①硫是淡黄色粉末,不溶于水;
②过氧化钠(Na2O2)是淡黄色粉末,溶于水并能与水反应,“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”
猜想与探究
猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物.
实验与结论
提出问题 过氧化钠是否为一种制氧剂?与人呼出的哪种气体发生反应?
提出猜想 过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气.
进行实验
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气. 王轩同学设计如图Ⅰ所示装置:
(1)实验现象及结论:观察到______现象,判断过氧化钠与氮气没有发生反应.
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气. 华宇同学设计了如下图所示装置
(2)其中A装置的作用是______.
(3)实验现象及结论:带火星的木条复燃;查阅资料知道:过氧化钠与水蒸气生成了氧气和一种常见碱,写出该反应的化学方程式______.
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气.
李杰在老师的指导下也设计了如图Ⅱ所示装置.(不考虑稀盐酸的挥发)
(4)实验记录
实验反思
(1)张红同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是______.请你回答如何改进该实验______.
(2)王兵同学查阅资料后知道实验Ⅲ中过氧化钠与二氧化碳反应生成碳酸钠和氧气,他称取过氧化钠与二氧化碳充分反应后的固体剩余物质21.5g,加入到盛有足量稀盐酸的烧杯中,并不断用玻璃棒搅拌.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图Ⅳ所示(不考虑实验过程中其它因素的影响).
请计算碳酸钠的质量分数:______.(写出计算过程,结果保留一位小数)
提出问题 这种淡黄色粉末是什么?有什么性质和用途?
查阅资料 ①硫是淡黄色粉末,不溶于水;
②过氧化钠(Na2O2)是淡黄色粉末,溶于水并能与水反应,“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”
猜想与探究
猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物.
实验与结论
| 实验操作 | 实验现象 | 实验结论 | |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水,充分振荡 | ______ | 猜想a、c不成立,猜想b成立. |
提出猜想 过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气.
进行实验
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气. 王轩同学设计如图Ⅰ所示装置:

(1)实验现象及结论:观察到______现象,判断过氧化钠与氮气没有发生反应.
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气. 华宇同学设计了如下图所示装置
(2)其中A装置的作用是______.
(3)实验现象及结论:带火星的木条复燃;查阅资料知道:过氧化钠与水蒸气生成了氧气和一种常见碱,写出该反应的化学方程式______.
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气.
李杰在老师的指导下也设计了如图Ⅱ所示装置.(不考虑稀盐酸的挥发)
(4)实验记录
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. | 装置的气密性良好. | |
| ② | 打开分液漏斗活塞,向A 装置中缓慢加入稀盐酸. | A装置中观察到的现象有______, C装置中有气泡出现. | A装置中发生反应的化学方程式为______; C装置作用是______. |
| ③ | 一段时间后用带火星的木条在D内进行检验. | 带火星的木条复燃. | 过氧化钠与二氧化碳反应并生成氧气. |
(1)张红同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是______.请你回答如何改进该实验______.
(2)王兵同学查阅资料后知道实验Ⅲ中过氧化钠与二氧化碳反应生成碳酸钠和氧气,他称取过氧化钠与二氧化碳充分反应后的固体剩余物质21.5g,加入到盛有足量稀盐酸的烧杯中,并不断用玻璃棒搅拌.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图Ⅳ所示(不考虑实验过程中其它因素的影响).
请计算碳酸钠的质量分数:______.(写出计算过程,结果保留一位小数)