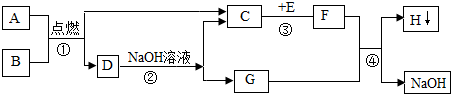
题目内容
4.实验探究:稀盐酸中哪一种粒子(H2O、H+、Cl-)能使指示剂变色.实验步骤:
(1)在甲试管中加入约2mL蒸馏水,滴入几滴紫色石蕊试液,观察现象.
(2)在乙试管中加入约2mL NaCl溶液,滴入几滴紫色石蕊试液,观察现象.
(3)在丙试管中加入约2mL 稀盐酸,滴入几滴紫色石蕊试液,观察现象.
通过上述实验,回答下列问题:
实验(1)看到的现象是溶液无变化,你得出的结论是H2O不能使石蕊变色;
实验(2)看到的现象是溶液无变化,你得出的结论是Cl-不能使石蕊变色;
实验(3)看到的现象是紫色石蕊试液变红,你得出的结论是H+使石蕊变色.
分析 石蕊试液遇酸性溶液变红色,遇中性溶液不变色,遇碱性溶液变蓝.
解答 解:①因为酸能使紫色石蕊变红,中性物质不能使紫色石蕊变色,蒸馏水是由水分子构成的.所以在第一支洁净的试管里加入约2mL蒸馏水,滴人几滴紫色石蕊试液,观察到的现象是颜色无变化,说明H2O分子不能使石蕊变色;
②氯化钠溶液呈中性,含有Na+Cl-滴入几滴紫色石蕊试液不变色,说明这两种微粒都不能使紫色石蕊试液变色;
③盐酸能使紫色石蕊变红色,由前两个实验知H2O分子和Cl-都不能使紫色石蕊试液变红色,而在盐酸中只含有H+Cl-和H2O分子三种微粒,所以只有H+能使紫色石蕊试液变红色;
故答案为:
①溶液无变化;H2O不能使石蕊变色;
②不能使石蕊变色;
③紫色石蕊试液变红; H+使石蕊变色
点评 本题以实验探究的方式来考查酸溶液使石蕊变红的原因,学生应注重实验中现象的观察,将现象和粒子结合来分析解决问题,从而得出正确的结论,学生应注重探究的学习过程.

练习册系列答案
相关题目
15.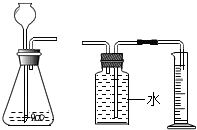 为了探究金属与酸反应的速率与哪些因素有关,小谷进行了以下实验探究:
为了探究金属与酸反应的速率与哪些因素有关,小谷进行了以下实验探究:
【实验方案】
【发现问题】在同一反应中其速率也不一样.
【继续探究】
小谷对锌粉与稀硫酸反应过程中速率的变化情况进行探究.
在100mL稀硫酸中加入足量的锌粉,用下图装置收集并测量氢气体积,记录的实验数据如下表:
【讨论】
(1)实验中测定反应产生氢气体积的实验装置如图,其中量筒的作用是根据进入量筒中水的体积,判断生成氢气的体积.
(2)实验数据反映,锌与稀硫酸反应的速率是先逐渐加快,一定时间后反应速率逐渐减慢,其原因是随着反应的进行,硫酸的浓度变小,反应速率变慢.
(3)若反应太剧烈了,操作难以控制,为了减缓反应速率但又不减少产生氢气的质量,可在硫酸溶液中加入适量的AB(多选)
A.蒸馏水 B.Na2SO4溶液 C.Na2CO3溶液 D.CuO.
 为了探究金属与酸反应的速率与哪些因素有关,小谷进行了以下实验探究:
为了探究金属与酸反应的速率与哪些因素有关,小谷进行了以下实验探究:【实验方案】
| 实验步骤 | 现象 | 结论 |
| ①将足量铁粉与锌粉分别放入10%100mL稀硫酸中,观察现象 | 产生气泡速率: Fe>Zn | 反应速率与反应物的金属的活动性强弱有关 |
| ②将等质量锌粉与锌片分别放入10%100mL稀硫酸中,观察现象 | 产生气泡速率: 锌粉>锌片 | 反应速率与反应物的接触面积大小有关 |
【继续探究】
小谷对锌粉与稀硫酸反应过程中速率的变化情况进行探究.
在100mL稀硫酸中加入足量的锌粉,用下图装置收集并测量氢气体积,记录的实验数据如下表:
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积 | 50 | 120 | 232 | 290 | 310 |
(1)实验中测定反应产生氢气体积的实验装置如图,其中量筒的作用是根据进入量筒中水的体积,判断生成氢气的体积.
(2)实验数据反映,锌与稀硫酸反应的速率是先逐渐加快,一定时间后反应速率逐渐减慢,其原因是随着反应的进行,硫酸的浓度变小,反应速率变慢.
(3)若反应太剧烈了,操作难以控制,为了减缓反应速率但又不减少产生氢气的质量,可在硫酸溶液中加入适量的AB(多选)
A.蒸馏水 B.Na2SO4溶液 C.Na2CO3溶液 D.CuO.
12.下列物质能使紫色石蕊试液变红的是( )
| A. | Fe2O3 | B. | KOH | C. | NaCl | D. | H2SO4 |
14.对下列化学用语中数字“2”的说法正确的是( )
①2N
②2CH4
③SO2
④$\stackrel{+2}{Ca}O$
⑤Fe2+
⑥2NO3-
⑦H2O.
①2N
②2CH4
③SO2
④$\stackrel{+2}{Ca}O$
⑤Fe2+
⑥2NO3-
⑦H2O.
| A. | 表示离子个数的是⑤⑥ | B. | 表示离子所带电荷数的是④⑤ | ||
| C. | 表示分子中原子个数的是③⑦ | D. | 表示分子个数的是①② |