题目内容
高纯的单晶硅是重要的半导体材料。制备高纯硅的化学方程式为:SiCl4+2H2 Si+4HCl。请计算要获得56g硅(Si),至少需要氢气多少克?
Si+4HCl。请计算要获得56g硅(Si),至少需要氢气多少克?
 Si+4HCl。请计算要获得56g硅(Si),至少需要氢气多少克?
Si+4HCl。请计算要获得56g硅(Si),至少需要氢气多少克?解:设至少需要氢气的质量为x。
SiCl4+2H2 Si+4HCl
Si+4HCl
2×2 28
x 56g
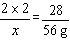
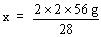 =8g
=8g
答:至少需要8g氢气。
SiCl4+2H2
 Si+4HCl
Si+4HCl2×2 28
x 56g
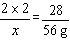
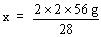 =8g
=8g答:至少需要8g氢气。

练习册系列答案
相关题目
 iCl4 +2H2高温 Si+ 4HCl。请计算要获得56g硅(Si),至少需要氢气的质量。
iCl4 +2H2高温 Si+ 4HCl。请计算要获得56g硅(Si),至少需要氢气的质量。