题目内容
14.下列说法正确的是( )| A. | 用水区别NaOH、Na2CO3两种固体 | |
| B. | 除去NaCl中的Ca2+和SO42-,可以先加入过量的Na2CO3,再加入过量的BaCl2 | |
| C. | 用稀硫酸除去Ca(OH)2中的CaCO3 | |
| D. | 可以用点燃的方法除去CO2中的CO |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
鉴别物质时,首先对需要鉴别的物质的性质进行对比分析找出特性,再根据性质的不同,选择适当的试剂,出现不同的现象的才能鉴别.
解答 解:A、NaOH溶于水放出大量的热,溶液的温度升高;碳酸钠溶于水温度变化不大,用水可以区别,故选项所采取的方法正确.
B、除去NaCl中的Ca2+和SO42-,先加入过量的Na2CO3,钙离子能与碳酸钠反应生成碳酸钙沉,再加入过量的BaCl2,过量的碳酸钠能与氯化钡反应生成碳酸钡沉淀,硫酸根离子能与氯化钡反应生成硫酸钡沉淀,能除去杂质但引入了新的杂质氯化钡(过量的,即引入了钡离子),不符合除杂原则,故选项所采取的方法错误.
C、CaCO3和Ca(OH)2均能与稀硫酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、除去二氧化碳中的一氧化碳不能够点燃,这是因为当二氧化碳(不能燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的;故选项所采取的方法错误
故选:A.
点评 物质的鉴别、分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.复合肥可以为农作物提供多种营养元素,下列化学肥料属于复合肥的是( )
| A. | Ca(H2PO4)2 | B. | KNO3 | C. | K2SO4 | D. | CO(NH2)2 |
5.下列事实不能用金属的活动性顺序加以解释的是( )
| A. | 不能用铜与稀硫酸反应制取氢气 | |
| B. | 铁能置换出硫酸铜溶液中的铜 | |
| C. | 在化合物中,铁显+2、+3价,铜显+1、+2价 | |
| D. | 相同条件下,锌和铁与稀硫酸反应的剧烈程度 |
2.某反应的微观示意图如下,下列说法正确的是( )
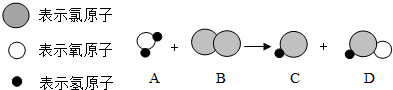

| A. | 该反应说明原子在化学反应中可再分 | |
| B. | 反应物的分子个数比为3:2 | |
| C. | 所有参与反应的物质都是化合物 | |
| D. | D物质中氯元素的化合价+1 |
9.下列用途正确的是( )
| A. | 生石灰可做某些气体的干燥剂 | |
| B. | 混合施用硫酸铵和草木灰(碳酸钾的水溶液呈碱性)可增强肥效 | |
| C. | 氧气可做火箭燃料 | |
| D. | 含磷衣粉粉含有植物生长所需的磷元素,提倡大量使用 |
19.下列饮品属于溶液的是( )
| A. | 蔗糖水 | B. | 牛奶 | C. | 果粒橙 | D. | 豆浆 |
6.下列物质的用途中,利用其化学性质的是( )
| A. | 干冰用于人工降雨 | B. | 天然气用作燃料 | ||
| C. | 液氮用作冷冻剂 | D. | 银用于制作导线 |
3.下列家庭小实验不能成功的是( )
| A. | 用食盐水浸泡菜刀除去表面的铁锈 | B. | 用闻气味的方法区别白酒和白醋 | ||
| C. | 用燃烧的方法区别羊毛和涤纶 | D. | 用肥皂水区别软水和硬水 |
4.下列叙述、对应的化学方程式、所属基本反应类型都正确的是( )
| A. | 服用含氢氧化铝的药物治疗胃酸过多 Al(OH)3+3HCl═AlCl3+3H20 复分解反应 | |
| B. | 拉瓦锡研究空气成分 2HgO$\frac{\underline{\;△\;}}{\;}$2Hg+O2 分解反应 | |
| C. | 用天然气作燃料 CH4+O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 | |
| D. | 验证铜和铝的活动性 3Cu+Al2(SO4)3═3CuSO4+2Al 置换反应 |