题目内容
2.元素周期表是学习和研究化学的重要工具,它的内容十分丰富.下表是依据元素周期表画出的1号~18号元素的原子结构示意图.请对它进行研究:
(1)上图中硫元素的相对原子质量近似为32,那么一个硫原子含中子16个,其核电荷数z=16,氯元素的原子最外层电子数y=7.
(2)核电荷数为12的元素的原子得到两个电子后,形成的粒子的符号是Mg2+,它的核外电子排布与氖元素的原子核外电子排布相同.
(3)上图的元素排列具有一定的规律:
①同一纵行中各元素的原子在结构上的相同点是最外层电子数,不同点是电子层数.
②同一横行中各元素的原子在结构上的相同点是电子层数,不同点是最外层电子数.
③根据以上规律,请推测一下,位于钠正下方的元素的原子结构示意图为
 .
.
分析 (1)根据相对原子质量≈质子数+中子数分析;根据原子中,原子序数=核电荷数=质子数=核外电子数来分析;
(2)根据离子符号的表示法:在元素符号的右上角标明离子所带电荷数及电性,及离子示意图找出相同的结构,进行解答;
(3)根据图中所给的信息及其规律进行解分析解答本题.
解答 解:(1)相对原子质量=质子数+中子数,所以硫原子内的中子数=32-16=16;Z=2+8+6=16;y=17-2-8=7;故填:16;16;7;
(2)根据离子符号的表示法:在元素符号的右上角标明离子所带电荷数及电性,所以核电荷数为12的元素的原子失去两个电子后,形成的粒子的符号为:Mg2+,它的核外电子排布与Ne元素的原子核外电子排布相同;故填:Mg2+;氖;
(3)根据图中所给的信息及其元素周期律可得:同一周期的元素具有相同的电子层数,但是最外层电子数不同;同一族的元素具有相同的最外层电子数,但是电子层数不同.
根据以上规律,请推测一下,位于钠正下方的元素的原子结构是,电子数层数比钠原子多一层,最外层电子数相同.
故答案为:①最外层电子数;电子层数;
②电子层数;最外层电子数;
③位于钠正下方的元素的原子结构有4个电子层,最外层有1个电子,是钾原子,故填: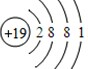 .
.
点评 本题主要考查了原子的结构示意图的意义,培养学生分析信息寻找规律以及解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
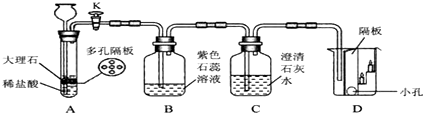
13.下列实验现象的描述,正确的是( )
| A. | 电解水时与正极相连的一端产生气泡速度快 | |
| B. | 硫在氧气中燃烧生成二氧化硫 | |
| C. | 红磷在氧气中燃烧产生大量白色烟雾 | |
| D. | 铁丝在氧气中燃烧火星四射,放热,生成黑色物质 |
14.下列说法错误的是( )
| A. | 煤的干馏和石油的分馏均属于物理变化 | |
| B. | 电解水时加氢氧化钠是为了增强水的导电性 | |
| C. | 厨房煤气管道漏气,立即关闭阀门并开窗通风 | |
| D. | 若不慎将燃着的酒精灯碰倒,洒出的酒精在桌上燃烧,应立刻用湿抹布扑盖 |
 元素周期表是学习和研究化学的重要工具.回答下列问题:
元素周期表是学习和研究化学的重要工具.回答下列问题: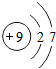 氟原子在化学反应中易得到(填“得到”或“失去”)电子变成离子,其离子符号为F-,由钠元素和氟元素组成的化合物氟化钠的化学式为NaF.
氟原子在化学反应中易得到(填“得到”或“失去”)电子变成离子,其离子符号为F-,由钠元素和氟元素组成的化合物氟化钠的化学式为NaF.