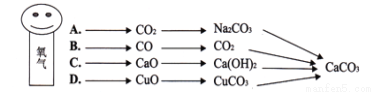
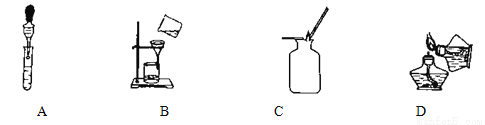
题目内容
某小组提纯含有泥沙的粗盐,并用提纯后的氯化钠来配制 100g 质量分数为 7.5%的 NaCl 溶液。
(1)粗盐提纯:
①将粗盐加入到盛有水的烧杯里,使用玻璃棒搅拌,作用是_____
②在蒸发结晶的过程中,当蒸发皿中_________停止加热。
(2)配制溶液:
③配制上述溶液需要称取提纯后的精盐____________g;
④量取所需的水应选用____________mL的量筒。
搅拌,加速溶解 出现较多固体时 7.5 100 【解析】(1)①溶解过程中玻璃棒的作用是搅拌,加速溶解;②在食盐溶液蒸发结晶的过程中,当蒸发皿中出现较多量固体时即停止加热,用余温蒸干剩余的液体; (2)③配制 100g 质量分数为 7.5%的 NaCl 溶液需要氯化钠的质量为100g ×7.5%=7.5g;④溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-7.5g=92.5g(...
练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
下列关于物质除杂所选用方法正确的是( )
选项 | 物质 | 所含杂质 | 除杂方法 |
A | FeSO4 溶液 | CuSO4 | 加入过量 Fe 粉并过滤 |
B | CO2 | CO | 将混合气体通过红热铜网 |
C | NaCl 溶液 | BaCl2 | 加入过量的Na2SO4 并过滤 |
D | Mg | Cu | 加入过量的稀硫酸并过滤 |
A. A B. B C. C D. D
A 【解析】A、过量Fe粉能与CuSO4溶液反应生成硫酸亚铁溶液和铜,能除去杂质且没有引入新的杂质,符合除杂原则,正确;B、铜与一氧化碳不反应,不能将二氧化碳中的一氧化碳除去,错误;C、BaCl2能与过量的Na2SO4溶液反应生成硫酸钡沉淀和氯化钠,能除去杂质,但引入了新的杂质硫酸钠(过量的),不符合除杂原则,错误;D、镁能与硫酸反应生成硫酸镁和氢气,铜不与稀硫酸反应,反而会把原物质除去,不...向一杯CaCl2溶液中分次、连续加入纯碱溶液,每次加入的纯碱溶液质量与每次产生沉淀质量的关系如下表所示,下列说法中正确的是
每次加入纯碱溶液质量/g | 20 | 10 | 10 | 5 |
每次产生沉淀质量/g | 8a | 4a | m | n |
A. 若m=2a,则n=a B. 若n=a,则m=2a
C. 若n=0,则m=0 D. 若m=0,则n=0
D 【解析】A. 若m=2a,第三次加入10g纯碱溶液,说明CaCl2溶液不足,则n=0,错误;B. 若n=a,第四次加入5g纯碱溶液,CaCl2溶液不足,则第三次加入纯碱溶液时,CaCl2溶液有剩余,所以m=4a,错误;C. 若n=0,是第三次加入纯碱溶液时,CaCl2溶液完全反应无剩余,m不一定为零,错误;D. 若m=0,是第二次加入10g纯碱溶液时,CaCl2溶液完全反应无剩余,则n=...