题目内容
18. 钙是维持人体正常功能所必需的元素,如图为某种补钙剂“钙尔奇”说明书的一部分
钙是维持人体正常功能所必需的元素,如图为某种补钙剂“钙尔奇”说明书的一部分取一片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其他成分与盐酸不反应),烧杯内物质质量变为11.34g.试计算:
(1)每片钙尔奇中含碳酸钙的质量.
(2)所用稀盐酸中溶质的质量分数.
分析 (1)欲正确解答本题,须根据盐酸与碳酸钙反应的化学方程式,得出各物质之间的质量比,列出比例式,即可求出每片钙尔奇中含碳酸钙的质量;
(2)由(1)已计算出10g盐酸中HCl的质量,根据溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%即可计算出所用盐酸中HCl的质量分数.
解答 解:(1)设每片钙尔奇中CaCO3的质量为x,10g盐酸中HCl的质量为y.
完全反应后产生的二氧化碳的质量为:2g+10g-11.34g=0.66g
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 0.66g
$\frac{100}{x}=\frac{73}{y}=\frac{44}{0.66g}$
x=1.5g
y=1.095g
(2)所用盐酸中HCl的质量分数为:$\frac{1.095g}{10g}$×100%=10.95%.
答:(1)每片钙尔奇中含碳酸钙的质量为1.5g;(2)所用稀盐酸中溶质的质量分数为10.95%.
点评 本题主要考查学生运用化学方程式和溶质质量分数公式进行计算的能力.学生需认真分析已知条件中的数量关系,正确书写化学方程式,才能解答.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
5.下列曲线图能正确表达相应反应或过程的是( )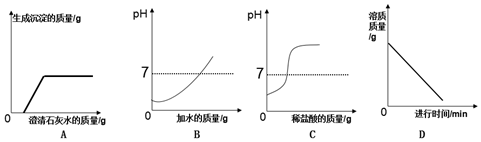

| A. | 一个烧杯中盛有稀盐酸和氯化镁溶液,滴加澄清石灰水 | |
| B. | 将 pH=1 的溶液加水稀释 | |
| C. | 向一定质量的 NaOH 溶液中滴入稀盐酸 | |
| D. | 向澄清石灰水中加入一定量的生石灰 |
2.表面部分被氧化的镁条2.6g,与某浓度的50g稀硫酸恰好完全反应,生成0.2g氢气.该稀硫酸的质量分数是( )
| A. | 20.58% | B. | 19.6% | C. | 98% | D. | 22.86% |
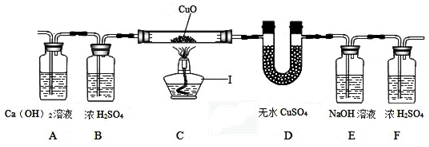
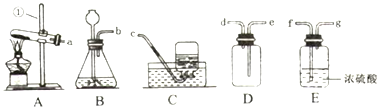
 世园会植物馆号称亚洲第一大钢结构管,拼装钢材杆件达到14000多根,所有杆件均为现场拼装焊接.
世园会植物馆号称亚洲第一大钢结构管,拼装钢材杆件达到14000多根,所有杆件均为现场拼装焊接.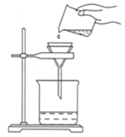 2016年我省某市初中化学实验操作技能考察中,小强同学抽到的试题是“水的净化”,请你与小强一起实验,并回答下列问题.
2016年我省某市初中化学实验操作技能考察中,小强同学抽到的试题是“水的净化”,请你与小强一起实验,并回答下列问题.