题目内容
10.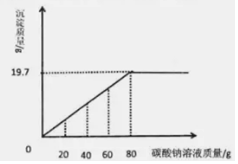 实验室有一包氯化钡和氯化钠的固体混合物32.5g,完全溶于141.2g水中,向其中逐滴加入碳酸钠溶液,反应过程中生成沉淀等质量与所加碳酸钠溶液质量的关系如图所示.
实验室有一包氯化钡和氯化钠的固体混合物32.5g,完全溶于141.2g水中,向其中逐滴加入碳酸钠溶液,反应过程中生成沉淀等质量与所加碳酸钠溶液质量的关系如图所示.计算:
(1)所用碳酸钠溶液的溶质质量分数;
(2)恰好完全反应时,所得溶液的溶质质量分数.
分析 题目给出了生成的碳酸钡的质量,根据碳酸钡的质量和对应的化学方程式求算碳酸钠的质量、氯化钡的质量和生成的氯化钠的质量,进而求算所用碳酸钠溶液的溶质质量分数和所得溶液中溶质氯化钠的质量分数.
解答 解:由图可以看出生成的碳酸钡的质量为19.7g
设参加反应的碳酸钠的质量为x,氯化钡的质量为y,生成氯化钠的质量为z
Na2CO3+BaCl2═BaCO3↓+2NaCl
106 208 197 117
x y 19.7g z
$\frac{106}{x}=\frac{208}{y}=\frac{197}{19.7g}=\frac{117}{z}$
x=10.6g,y=20.8g,z=11.7g
所用碳酸钠溶液的溶质质量分数$\frac{10.6g}{80g}×100%$=13.25%,
反应后溶液中NaCl的质量分数为:$\frac{32.5g-20.8g+11.7g}{32.5g+141.2g+80g-19.7g}×100%$=10%
答:(1)所用碳酸钠溶液的溶质质量分数为13.25%,
(2)恰好完全反应时,所得溶液中溶质的质量分数是10%.
点评 反应后溶液的质量可根据质量守恒定律求得,反应后所得溶液质量=混合物质量+所加水质量+所加入氯化钡溶液质量-生成硫酸钡沉淀质量,可以使溶液质量的计算更为简单明了.

练习册系列答案
相关题目
1.如图所示,甲和乙在一定条件下反应生成丙和丁.
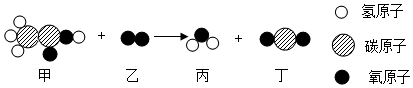
关于该反应,下列说法正确的是( )

关于该反应,下列说法正确的是( )
| A. | 反应生成的丙和丁的质量比是9:22 | B. | 该反应中氧元素化合价不发生改变 | ||
| C. | 四种物质都是氧化物 | D. | 该反应属于置换反应 |
15.关于反应C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+2X↑+2H2O,下列分析错误的是( )
| A. | X气体排放到空气中,会造成空气污染 | |
| B. | 硫元素的化合价在化学反应前后没有发生改变 | |
| C. | 硫酸中硫元素与氧元素的质量比为1:2 | |
| D. | 该反应说明了碳具有还原性,浓硫酸具有氧化性 |
2.除去下列物质中含有的杂质,所选用的试剂和方法错误的是( )
| 物质 | 杂质 | 所加试剂 | 主要方法 | |
| A | H2O | 悬浮物 | 明矾 | 吸附 |
| B | NaNO3溶液 | NaCl | 过量AgNO3溶液 | 过滤 |
| C | CO | CO2 | NaOH | 干燥 |
| D | Ag | Fe | 稀盐酸 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
11.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
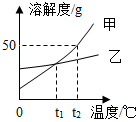

| A. | 甲的溶解度大于乙的溶解度 | |
| B. | t2℃时,甲饱和溶液溶质质量分数为50% | |
| C. | t1℃时,甲、乙两种物质的溶液中,溶质质量分数相等 | |
| D. | 将t2℃时等质量甲、乙的饱和溶液分别降至t1℃,所得溶液中的溶剂质量:甲<乙 |
 )与B(
)与B( )反应生成C(
)反应生成C( ),如图是其反应前后分子及其数目变化的微观示意图
),如图是其反应前后分子及其数目变化的微观示意图 和
和 表示两种质子数不同的原子)
表示两种质子数不同的原子)
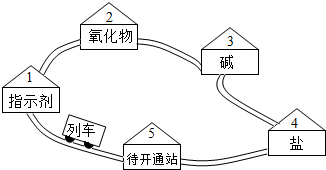 请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站.“2~5号站”各站的对应物质属于不同类别物质.
请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站.“2~5号站”各站的对应物质属于不同类别物质.