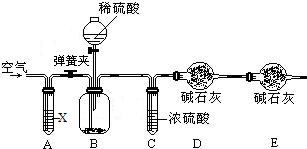
题目内容
现有11克氯化钠和碳酸钠混合样品,加入100克稀盐酸恰好完全反应,生成106.6克不饱和溶液,求:(1)产生二氧化碳气体______ g.
(2)计算该样品中碳酸钠的质量分数.
(3)所得溶液溶质的质量分数.
【答案】分析:(1)跟据质量守恒定律可知反应物前后总物质减少的质量即为生成二氧化碳的质量.
(2)由二氧化碳的质量根据碳酸钠与盐酸反应的化学方程式可以计算出样品中碳酸钠的质量分数.
(3)反应后所得溶液为氯化钠溶液,而样品中的氯化钠不与盐酸反应;至完全反应后,所得溶液为氯化钠溶液,其溶质氯化钠由两部分组成:一部分为原混合物质中的氯化钠,另一部分则是反应生成的氯化钠,据此解答即可;
解答:解:(1)生成二氧化碳的质量为
11g+100g-106.6g=4.4g
(2)设样品中碳酸钠的质量为x,生成的氯化钠是y.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
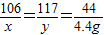
x=10.6g y=11.7g
碳酸钠的质量分数=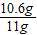 ×100%≈96.4%
×100%≈96.4%
(3)所得溶液中NaCl的质量为原样品中氯化钠的质量与生成氯化钠的质量之和.
氯化钠的质量=11.7g+(11g-10.6g)=12.1g
溶液的质量=106.6g
所得溶液的溶质质量分数=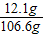 ×100%≈11.4%
×100%≈11.4%
故答案为:(1)4.4;(2)样品中碳酸钠的质量分数为96.4%;(3)反应后所得溶液中溶质的质量分数11.4%;
点评:此题是对化学方程式以及溶液相关问题的考查,利用质量守恒定律,计算出反应放出二氧化碳的质量是解决问题的基础.
(2)由二氧化碳的质量根据碳酸钠与盐酸反应的化学方程式可以计算出样品中碳酸钠的质量分数.
(3)反应后所得溶液为氯化钠溶液,而样品中的氯化钠不与盐酸反应;至完全反应后,所得溶液为氯化钠溶液,其溶质氯化钠由两部分组成:一部分为原混合物质中的氯化钠,另一部分则是反应生成的氯化钠,据此解答即可;
解答:解:(1)生成二氧化碳的质量为
11g+100g-106.6g=4.4g
(2)设样品中碳酸钠的质量为x,生成的氯化钠是y.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
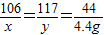
x=10.6g y=11.7g
碳酸钠的质量分数=
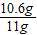 ×100%≈96.4%
×100%≈96.4%(3)所得溶液中NaCl的质量为原样品中氯化钠的质量与生成氯化钠的质量之和.
氯化钠的质量=11.7g+(11g-10.6g)=12.1g
溶液的质量=106.6g
所得溶液的溶质质量分数=
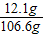 ×100%≈11.4%
×100%≈11.4%故答案为:(1)4.4;(2)样品中碳酸钠的质量分数为96.4%;(3)反应后所得溶液中溶质的质量分数11.4%;
点评:此题是对化学方程式以及溶液相关问题的考查,利用质量守恒定律,计算出反应放出二氧化碳的质量是解决问题的基础.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目