题目内容
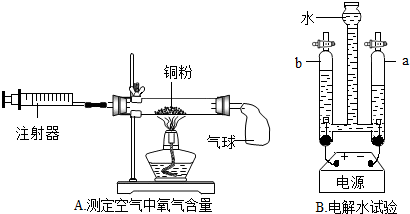
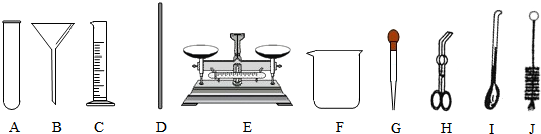
某研究性学习小组利用下列装置进行气体的制取实验,请分析回答下列问题.

(1)写出标号①和②仪器的名称:① ② ;
(2)实验室用氯酸钾和二氧化锰制取氧气的装置组合为 ;二氧化锰在反应中作用是 ,它的质量百分含量在反应后 (“变大”,“变小”,“不变”)
(3)写出实验室用B E装置组合制取气体的化学反应方程式为 ,若将标号①仪器换成分液漏斗,实验目的是 .
(4)若用F装置收集氧气,检验氧气是否集满的方法是 .若用F装置检验制得的气体是否为二氧化碳,则在F装置中放入一定量的 .

(1)写出标号①和②仪器的名称:①
(2)实验室用氯酸钾和二氧化锰制取氧气的装置组合为
(3)写出实验室用B E装置组合制取气体的化学反应方程式为
(4)若用F装置收集氧气,检验氧气是否集满的方法是
考点:氧气的制取装置,氧气的收集方法,氧气的检验和验满,催化剂的特点与催化作用,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)要熟悉各种仪器的名称、用途和使用方法;
(2)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
氧气的密度比空气的密度大,不易溶于水;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,氢气难溶于水,密度比空气小;
(4)氧气能够支持燃烧,能使带火星的木条复燃;
二氧化碳能使澄清石灰水变浑浊.
(2)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
氧气的密度比空气的密度大,不易溶于水;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,氢气难溶于水,密度比空气小;
(4)氧气能够支持燃烧,能使带火星的木条复燃;
二氧化碳能使澄清石灰水变浑浊.
解答:解:(1)①是长颈漏斗,通过长颈漏斗可以向反应容器中注入液体药品;②是水槽,常用于排水法收集气体.
故填:长颈漏斗;水槽.
(2)实验室用氯酸钾和二氧化锰制取氧气时需要加热,应该用A装置作为发生装置;
因为氧气的密度比空气大,可以用向上排空气法收集,即用D或F装置收集,氧气不易溶于水,可以用排水法收集,即用E装置收集;
二氧化锰在反应中作用是催化作用,因为二氧化锰在反应前后的质量不变,试管中的总质量变小,因此它的质量百分含量在反应后变大.
故填:AD或AE或AF;催化作用;变大.
(3)实验室用B、E装置组合制取的气体应该是氧气或氢气,反应的化学反应方程式分别为:2H2O2
2H2O+O2↑、Zn+H2SO4═ZnSO4+H2↑;
若将标号①仪器换成分液漏斗,通过分液漏斗可以控制液体药品的流量,从而可以控制反应速率.
故填:2H2O2
2H2O+O2↑,或Zn+H2SO4═ZnSO4+H2↑;控制反应速率.
(4)若用F装置收集氧气,检验氧气是否集满的方法是:将带火星的木条放在导管b口处,若木条复燃,则收集满;
若用F装置检验制得的气体是否为二氧化碳,则在F装置中放入一定量的澄清石灰水,二氧化碳能使澄清的石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:将带火星的木条放在导管b口处,若木条复燃,则收集满;澄清石灰水.
故填:长颈漏斗;水槽.
(2)实验室用氯酸钾和二氧化锰制取氧气时需要加热,应该用A装置作为发生装置;
因为氧气的密度比空气大,可以用向上排空气法收集,即用D或F装置收集,氧气不易溶于水,可以用排水法收集,即用E装置收集;
二氧化锰在反应中作用是催化作用,因为二氧化锰在反应前后的质量不变,试管中的总质量变小,因此它的质量百分含量在反应后变大.
故填:AD或AE或AF;催化作用;变大.
(3)实验室用B、E装置组合制取的气体应该是氧气或氢气,反应的化学反应方程式分别为:2H2O2
| ||
若将标号①仪器换成分液漏斗,通过分液漏斗可以控制液体药品的流量,从而可以控制反应速率.
故填:2H2O2
| ||
(4)若用F装置收集氧气,检验氧气是否集满的方法是:将带火星的木条放在导管b口处,若木条复燃,则收集满;
若用F装置检验制得的气体是否为二氧化碳,则在F装置中放入一定量的澄清石灰水,二氧化碳能使澄清的石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:将带火星的木条放在导管b口处,若木条复燃,则收集满;澄清石灰水.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知氯磺酸化学式为ClSO3H,能在水中完全电离出H+和ClSO3-;甲酸化学式为HCOOH,能在水中部分电离出H+和HCOO-.对于反应C1SO3H+HCOOH═CO↑+HCl+H2SO4有如下判断,其中合理的是( )
| A、此反应属于复分解反应 |
| B、此反应中碳元素的化合价发生改变 |
| C、反应前后溶液的总质量不变 |
| D、反应后溶液的pH减小 |
人类的发展史也是人类利用材料的历史,下列材料属于天然材料的是( )
| A、石器 | B、青铜器 |
| C、铁器 | D、计算机芯片 |
下列说法不正确的是( )
| A、氧气能支持燃烧,因为氧气具有可燃性 |
| B、常用氮气做食品保护气,因为氮气的化学性质不活泼 |
| C、氧气化学性质活泼,能与多种物质反应 |
| D、饼干在空气中放置一段时间后会变软,说明空气中含有水蒸气 |
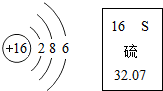 根据图中的信息判断,下列说法中正确的是( )
根据图中的信息判断,下列说法中正确的是( )| A、硫属于金属元素 |
| B、硫原子的核电荷数为16 |
| C、硫原子的相对原子质量为32.07 |
| D、在化学反应中,硫原子容易失去电子 |
下列说法你认为错误的是( )
| A、化学变化和化学反应是同一个概念 |
| B、物质发生化学变化时一定同时发生物理变化 |
| C、化学变化的特征就是一定会有沉淀或气体生成 |
| D、化学变化一定会产生新物质 |