题目内容
元素周期表是学习和研究化学的重要工具,它的内容十分丰富.如图是依据元素周期表画出的1-18号元素的原子结构示意图.请结合所学知识回答下列问题: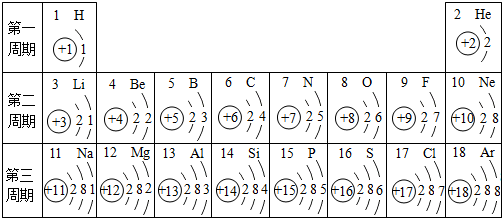
(1)原子序数为12的元素名称是 ,在化学反应中,该元素的原子容易 (填“得”或“失”)电子;原子序数为16的元素属于 元素(填“金属”或“非金属”).
(2) 元素与氯元素化学性质相似,该元素与钠元素形成的化合物的化学式为 .
(3)我发现如下规律:①原子序数与元素原子核电荷数在数值上相等;
② ;
③ .

(1)原子序数为12的元素名称是
(2)
(3)我发现如下规律:①原子序数与元素原子核电荷数在数值上相等;
②
③
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:(1)原子序数为17的元素为Cl,写出名称即可;根据原子结构示意图的特点:金属元素的最外层电子数一般少于4,易失去最外层电子形成阳离子;非金属元素的最外层电子数一般多于4,易得到电子,形成阴离子;进行解答;
(2)最外层电子数相同的化学性质相似,氯元素与氟元素的最外层电子数相同,故氯元素与氟元素的化学性质相似,根据化合价代数和为零的原则书写化学式;
(3)根据元素周期律及图表中的信息进行分析解答.
(2)最外层电子数相同的化学性质相似,氯元素与氟元素的最外层电子数相同,故氯元素与氟元素的化学性质相似,根据化合价代数和为零的原则书写化学式;
(3)根据元素周期律及图表中的信息进行分析解答.
解答:解:(1)原子序数为12的名称为镁; 根据原子结构示意图的特点:金属元素的最外层电子数一般少于4;易失去电子;原子序数为16的元素为氧元素,属于非金属元素;
(2)氯元素与氟元素的最外层电子数相同,故氯元素与氟元素的化学性质相似;根据在化合物中化合价代数和为零的原则,氟的化合价为--1价,钠的化合价为+1价,故形成的化合物的化学式为NaF;
(3)根据元素周期律及图表中的信息可总结:
电子层数等于周期数;同一纵行从上到下电子层数逐渐增加;同一纵行,原子最外层电子数相同;最右纵行的原子结构均为稳定结构;同一周期原子的最外层电子数从左到右逐渐增加;
答案:(1)镁; 失; 非金属; (2)F,NaF;
(3)②电子层数与元素所在周期数相等;
③同一周期最外层电子数依次增加.
(2)氯元素与氟元素的最外层电子数相同,故氯元素与氟元素的化学性质相似;根据在化合物中化合价代数和为零的原则,氟的化合价为--1价,钠的化合价为+1价,故形成的化合物的化学式为NaF;
(3)根据元素周期律及图表中的信息可总结:
电子层数等于周期数;同一纵行从上到下电子层数逐渐增加;同一纵行,原子最外层电子数相同;最右纵行的原子结构均为稳定结构;同一周期原子的最外层电子数从左到右逐渐增加;
答案:(1)镁; 失; 非金属; (2)F,NaF;
(3)②电子层数与元素所在周期数相等;
③同一周期最外层电子数依次增加.
点评:本题考查学生对元素周期律的理解与掌握,并能灵活应用的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列食物中,主要为人体提供糖类的是( )
A、 大米 |
B、 牛奶 |
C、 蔬菜 |
D、 花生 |
如图所示的实验操作中正确的是( )
A、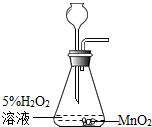 实验室制氧气 |
B、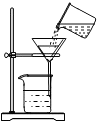 过滤 |
C、 取锌粒 |
D、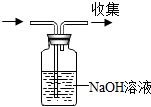 除去CO中少量CO2 |
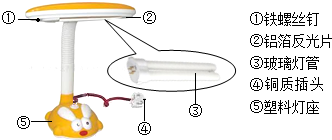 青少年看书、写字一定要爱护眼睛,台灯是在光线不足时常用的照明用具.
青少年看书、写字一定要爱护眼睛,台灯是在光线不足时常用的照明用具.  “嫦娥三号”于2013年12月2日,在西昌卫星发射中心发射,中国成为世界上第3个实现月球软着陆的国家.试回答:
“嫦娥三号”于2013年12月2日,在西昌卫星发射中心发射,中国成为世界上第3个实现月球软着陆的国家.试回答: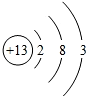 铝在工业和日常生活中应用广泛.请回答:
铝在工业和日常生活中应用广泛.请回答: