题目内容
16.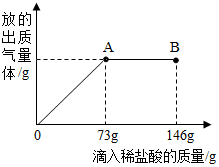 已知 Na2CO3溶液呈碱性.在一烧杯中盛有20.4g Na2CO3和NaCl组成的固体混合物,向其中逐渐滴加10%的稀盐酸.放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示.请回答:
已知 Na2CO3溶液呈碱性.在一烧杯中盛有20.4g Na2CO3和NaCl组成的固体混合物,向其中逐渐滴加10%的稀盐酸.放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示.请回答:(1)当滴加稀盐酸至图中B点时,烧杯中溶液的pH<7 (填>、=、<);
(2)当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出反应后所得溶液中溶质的质量分数.
分析 根据图示进行分析,当滴加稀盐酸到A点时,碳酸钠完全反应,反应后生成了氯化钠,原来的固体混合物中也有氯化钠,根据所用氯化氢的质量可求出固体混合物中的碳酸钠的质量,从而能求出固体混合物中氯化钠的质量,再加上反应后生成的氯化钠的质量就是反应后溶质的质量,而反应后溶液的质量为所加所以物质的质量减去生成的气体的质量.
解答 解:(1)由图可知,当滴加稀盐酸至A点时,物质完全反应,所以当滴加到B点时,盐酸过量,烧杯中溶液的PH<7;(2)设滴加稀盐酸到A时,放出气体的质量为X,参加反应的碳酸钠的质量为Y,生成的氯化钠的质量为Z
由题意可知,当滴加到A时,所用氯化氢的质量是73g×10%═7.3g
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
Y 7.3g Z X
$\frac{106}{Y}=\frac{73}{7.3g}=\frac{117}{Z}=\frac{44}{X}$
Y═10.6g
Z═11.7g
X═4.4g
溶质为氯化钠,氯化钠的质量为:11.7g+20.4g-10.6g═21.5g
溶液的质量为:20.4g+73g-4.4g═89g
所以溶质的质量分数为:$\frac{21.5g}{89g}$×100%═24.2%.
故答为:(1)<;(2)当滴加稀盐酸至图中A点时,溶质的质量分数为24.2%.
点评 本题在计算时,溶液质量的计算是关键,容易出错,应根据质量守恒,反应后溶液的质量=固体混合质量+加入稀盐酸质量-放出气体质量.

练习册系列答案
相关题目
4.用试管加热固体时,因操作不正确而出现试管炸裂的现象,其原因可能是( )
| A. | 加热前试管外壁干燥 | |
| B. | 没有预热,加热不均匀,局部温度过高 | |
| C. | 试管口略向下倾斜了 | |
| D. | 试管夹夹在试管中上部了 |
1.实验是学习化学的重要方法.以下关于实验的叙述中正确的是( )
| A. | 收集一集气瓶氢气,将带火星的木条放在集气瓶口验满 | |
| B. | 粗盐提纯过滤盐水时,还要用玻璃棒轻轻搅动漏斗中的液体 | |
| C. | 某溶液中加入用盐酸酸化了的氯化钡溶液有白色沉淀生成,说明有硫酸根 | |
| D. | 检验装置的气密性要在加放试剂之前进行 |
8.课外活动即第二课堂,是我们自由发展才智的新天地.某课外活动小组在实践调查时发现了下列一些现象,你认为其中合理的是( )
| A. | 现代农业按照国家标准,适量使用化肥、农药 | |
| B. | 用甲醛溶液浸泡水产品,可以起到防腐作用 | |
| C. | 将工业明胶代替食用明胶,添加到老酸奶、果冻中 | |
| D. | 将工厂的烟囱造高,以减少工厂周围的大气污染 |