题目内容
人类对金属的开发和利用是循序渐进的.
(1)青铜器是人类较早使用的金属制品.西汉时期,人们主要采用“湿法冶金”.如将铁浸入硫酸铜溶液中,可以制得铜,这是因为铁的金属活动性比铜 (填“强”或“弱”).
(2)随着技术的不断进步,人们能利用还原剂从金属的氧化物中将其还原出来.例如,高炉炼铁所涉及的物质转化过程如图:

其中A与赤铁矿中的氧化铁反应的化学方程式为 .
(3)每年因为腐蚀(如铁生锈)而报废的金属相当于年产量的20%~40%,人们采用多种方法防止金属腐蚀.例如,将清洗后的铁锅擦干后存放可以防止铁锅生锈,其原因是 .
(1)青铜器是人类较早使用的金属制品.西汉时期,人们主要采用“湿法冶金”.如将铁浸入硫酸铜溶液中,可以制得铜,这是因为铁的金属活动性比铜
(2)随着技术的不断进步,人们能利用还原剂从金属的氧化物中将其还原出来.例如,高炉炼铁所涉及的物质转化过程如图:

其中A与赤铁矿中的氧化铁反应的化学方程式为
(3)每年因为腐蚀(如铁生锈)而报废的金属相当于年产量的20%~40%,人们采用多种方法防止金属腐蚀.例如,将清洗后的铁锅擦干后存放可以防止铁锅生锈,其原因是
考点:金属的化学性质,铁的冶炼,金属锈蚀的条件及其防护,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据金属与盐反应需要满足的条件考虑;
(2)根据炼铁的过程及原理进行分析解答即可;
(3)依据钢铁生锈的条件判断防锈的方法即可;
(2)根据炼铁的过程及原理进行分析解答即可;
(3)依据钢铁生锈的条件判断防锈的方法即可;
解答:解:(1)金属与盐反应时,金属要排在盐中金属的前边,反应物中盐溶于水,金属不能是钾、钙、钠,所以将铁浸入硫酸铜溶液中,可以制得铜,说明铁比铜活泼;
(2)一氧化碳与氧化铁反应的反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,用观察法配平,反应条件是高温,所以方程式是:Fe2O3+3CO
2Fe+3CO2;
(3)钢铁生锈的条件是与水和氧气接触,故将清洗后的铁锅擦干可以防止铁与水接触,从而达到铁锅防锈的目的.
故答案为:(1)强;(2)Fe2O3+3CO
2Fe+3CO2;(3)防止铁与水接触.
(2)一氧化碳与氧化铁反应的反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,用观察法配平,反应条件是高温,所以方程式是:Fe2O3+3CO
| ||
(3)钢铁生锈的条件是与水和氧气接触,故将清洗后的铁锅擦干可以防止铁与水接触,从而达到铁锅防锈的目的.
故答案为:(1)强;(2)Fe2O3+3CO
| ||
点评:本题是一道金属知识的考查题,从金属的利用,冶炼,锈蚀及保存等方面全面考查了金属的性质,是一道不错的试题.

练习册系列答案
相关题目
下列属于化学反应的是( )
| A、海水晒盐 | B、牛奶变酸 |
| C、人工降雨 | D、风力发电 |
为减缓化学反应速率,下列做法合理的是( )
| A、面团发酵时放在温热处 |
| B、在食品密封包装时充入氮气 |
| C、煤燃烧时向煤炉中鼓入空气 |
| D、用食醋除水垢时使用浓度高的食醋 |

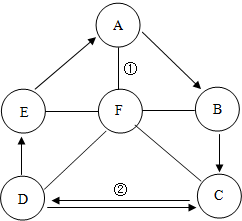 A~F均为初中所学的物质.其中属于碱的是B、C,属于盐的是D、E,其中D是钠盐;胃酸中含有F能帮助消化,A是食品包装袋中常用的干燥剂.其物质间的转化关系如图所示.图中“-”表示两端的物质能发生反应;“→”表示物质间存在转化关系,其余反应条件、部分反应物和生成物均已略去.试回答:
A~F均为初中所学的物质.其中属于碱的是B、C,属于盐的是D、E,其中D是钠盐;胃酸中含有F能帮助消化,A是食品包装袋中常用的干燥剂.其物质间的转化关系如图所示.图中“-”表示两端的物质能发生反应;“→”表示物质间存在转化关系,其余反应条件、部分反应物和生成物均已略去.试回答: