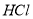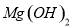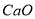题目内容
(6分)为了测定某石灰石样品中碳酸钙的质量分数,某兴趣小组的同学进行了如下实验:取12.5g 石灰石样品,放入盛有100g稀盐酸的烧杯中,石灰石中的碳酸钙与盐酸恰好完全反应(假设石灰石中的杂质不与盐酸反应也不溶于水),烧杯内物质质量变为108.1g。
求:(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为 g.
(2)求该石灰石中碳酸钙的质量分数?
(3)将反应后的混合物过滤,求所得滤液的溶质质量分数?(计算结果保留一位小数)
(1)4.4克(2)80%(3)10.5%
【解析】
试题分析:根据质量守恒定律可以知道生成二氧化碳的质量=12.5克+100克-108.1克=4.4克,设碳酸钙的质量为X,生成的氯化钙的质量为Y,
CaCO3 + 2HCl==CaCl2 + CO2↑ + H2O
100 111 44
X Y 4.4克
列比例式得:100:X=44:4.4克 求得X=10克 石灰石中碳酸钙的质量分数=10/12.5×100%=80%
111:Y=44:4.4克 求得Y=11.1克滤液的质量=108.1克-(12.5克-10克)=105.6克滤液的溶质质量分数=11.1/105.6×100%=10.5%。
考点:质量守恒定律 根据化学方程式的计算 溶质质量分数

(2分)除去下列物质中的少量杂质,所选用的试剂和操作方法都正确的是
物质 | 杂质 | 试剂 | 操作方法 | |
A |
|
| 硝酸钡溶液 | 加水溶解,再加适量硝酸钡溶液,过滤,将滤液蒸发结晶 |
B |
|
|
| 干燥 |
C |
|
| 过量 | 过滤 |
D |
| 石灰石 | 无 | 高温煅烧 |
A.A B.B C.C D.D
将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下:
物 质 | a | b | c | d |
反应前质量(g) | 6.4 | 3.2 | 4.0 | 0.5 |
反应后质量(g) | 待测 | 2.56 | 7.2 | 0.5 |
下列说法中错误的是:
A.a和b是反应物,d可能是催化剂。
B.反应后a物质的质量为3.84g
C.c物质中元素的种类,一定与a、b二种物质中元素的种类相同
D.若物质a与物质b的相对分子质量之比为2:1,则a与b的化学计量数之比为3:1
下列实验操作不能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 除去CO2中少量的CO | 将混合气体通过灼热的氧化铜 |
B | 鉴别Cu和Fe3O4 | 观察颜色 |
C | 鉴别H2O 和H2O2溶液 | 分别取少量液体于试管中,加入MnO2 |
D | 除去KNO3中少量的NaCl | 将混合物先溶解再过滤,然后蒸发结晶 |
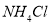
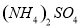
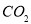
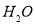
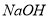 固体
固体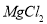 溶液
溶液