题目内容
2.海洋是巨大的资源宝库,从海洋中可以获得很多物质,连云港水资源丰富.(1)通过晾晒海水得到的粗盐中含有多种可溶性杂质和不溶性杂质(泥沙等).实验室中除去粗盐中不溶性杂质获得精盐的步骤是:溶解→过滤→蒸发→计算产率等.
①过滤操作中玻璃棒的末端要轻轻的斜靠在三层滤纸一边.蒸发时为防止液滴飞溅,除用玻璃棒搅拌外,还可以采取的操作是移走酒精灯.
②下列操作可能导致精盐产率偏高的是b(填字母)
a.食盐没有完全溶解即过滤 b.过滤时液面高于滤纸边缘
c.器皿上粘有的精盐没有全部转移到称量纸上
(2)海水中含量最多的氯化物是氯化钠,其次是氯化镁.如图1是从海水中获得氯化镁溶液的流程.
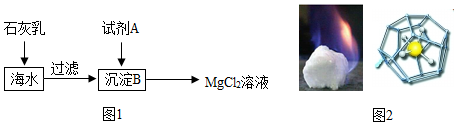
①在海水中加入石灰乳后,发生反应的化学方程式是MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2.
②上述过程中试剂A与沉淀B法神的是中和反应,则试剂A是(填名称)稀盐酸.
(3)2017年5月18日,在中国南海海域实现可燃冰(CH4•nH2O)试采成功,这将使人类能源格局翻开新篇章.
①可燃冰中,水分子形成一种空间笼状结构,甲烷和少量N2、CO2等分子填入笼内空隙中,无固定的化学计量关系,因此可燃冰属于混合物(选填“纯净物”或“混合物”).
②若某种可燃冰中CH4与H2O的质量比是1:9,则该可燃冰中n=8.
③可燃冰中甲烷完全燃烧的化学方程式是CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
分析 (1)①根据过滤时的注意事项解答;根据蒸发时的注意事项解答;
②如果操作不当,会影响实验结果,甚至会导致实验失败.
(2)①石灰乳与海水混合,氢氧化钙与氯化镁反应生成氢氧化镁沉淀和氯化钙,进行分析解答.
②氢氧化镁难溶于水,能与酸反应,据此进行分析解答.
(3)①根据题中信息分析解答;
②根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答;
③根据甲烷燃烧的原理以及化学方程式的写法来分析;
解答 解:
(1)过滤操作中,为防止弄破滤纸,玻璃棒的末端要轻轻的斜靠在三层滤纸一边.蒸发时为防止液滴飞溅,除用玻璃棒搅拌外,还可以采取的操作是移走酒精灯;
②a.食盐没有完全溶解即过滤,会导致部分精盐损失,从而导致制得的精盐的产率偏低;
b.过滤时液面高于滤纸边缘,会导致部分不溶于水的物质留在精盐中,从而导致制得的精盐的产率偏高;
c.器皿上粘有的精盐没有全部转移到称量纸上,会导致精盐质量偏小,从而导致制得的精盐的产率偏低;
(2)①石灰乳与海水混合,氢氧化钙与氯化镁反应生成氢氧化镁沉淀和氯化钙,反应的化学方程式为:MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2.
②氢氧化镁难溶于水,与稀盐酸反应能生成氯化镁和水,故试剂X为稀盐酸.
(3)①根据题中信息“天然气水合物中,水分子形成一种空间笼状结构,CH4和少量的N2、CO2等分子填入笼内的空隙中,无固定的化学计量关系”可知,天然气水合物中由水、甲烷、氮气、二氧化碳等组成,为一种混合物;
②根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得可燃冰分子中CH4与H2O的质量比为:(12+1×4):[n(1×2+16)=1:9;z则n=8;
③甲烷与氧气在点燃的条件下反应生成水和二氧化碳;化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
答案:
(1)①三层滤纸;移走酒精灯;
②b;
(2)①MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2.②稀盐酸;
(3)①混合物;
②8;
③CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案| A | B | C | D |
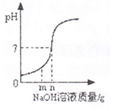 | 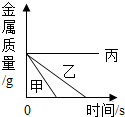 |  | 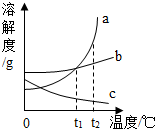 |
| 向盐酸中加入的氢氧化钠溶液为mg时,所得溶液显碱性 | 向三份完全相同的稀盐酸中分别加入甲、乙、丙三种金属,则甲、乙的金属活动性比丙的强 | 用等质量、等浓度的双氧水分别制取氧气 | 将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,所得溶液变成不饱和溶液 |
| A. | A | B. | B | C. | C | D. | D |
(1)填写下表空格处的化学式:
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| KCl | CaCl2 | NaCl | MgCl2 | AlCl3 | ZnCl2 | FeCl2 | CuCl2 |
(2)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了如图,请你在右边的圆圈中填入适当的化学式或离子符号:
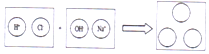
(3)稀盐酸和氢氧化钠之间发生的反应可称为复分解或中和反应.
| A. | 碘酒中的溶剂是酒精,溶质是碘 | |
| B. | 溶液中各部分性质相同,是一种均一、稳定的混合物 | |
| C. | 析出晶体的溶液是该溶质的饱和溶液 | |
| D. | 葡萄糖、植物油、蛋清都可溶于水形成溶液 |
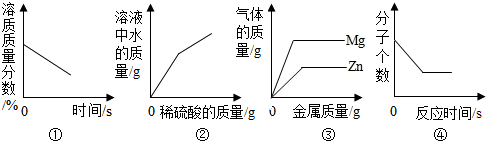
①将接近饱和的硝酸钾溶液缓慢降温
②向一定量的氢氧化钡溶液中加过量稀硫酸
③向等质量、等质量分数的稀盐酸中分别逐渐加入锌粉、镁粉至过量
④在密闭容器中点燃H2和O2的混合气体.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
①金刚石-C ②五氧化二磷-O5P2 ③氯化铁-FeCl2
④钠元素显+1价-Na+1 ⑤两个镁离子-2Mg2+.
| A. | ①②④ | B. | ②③⑤ | C. | ①⑤ | D. | ②③④ |
| A. | 酸 | B. | 碱 | C. | 有机物 | D. | 盐 |
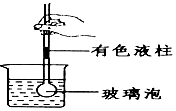 化学是一个神奇的世界,它可以带你体验物质与能量的变化,例如:
化学是一个神奇的世界,它可以带你体验物质与能量的变化,例如: