题目内容
6.实验是学习化学的重要手段.下列实验设计不能达到实验目的是( )| 选项 | 实验目的 | 实验设计[ |
| A | 确定NaOH溶液是否变质 | 滴加澄清石灰水观察现象 |
| B | 区别稀盐酸和稀硫酸 | 滴加氯化钡溶液观察现象 |
| C | 除去MnO2粉末中的KCl杂质 | 溶解、过滤、洗涤、干燥 |
| D | 检验Na2CO3溶液中是否含有NaCl杂质 | 滴加稀盐酸观察现象 |
| A. | A | B. | B | C. | C | D. | D |
分析 氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,碳酸钠能和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠;
稀盐酸和氯化钡不能反应,稀硫酸和氯化钡反应生成白色沉淀硫酸钡和稀盐酸;
二氧化锰不溶于水,氯化钾易溶于水;
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,氯化钠不能和稀盐酸反应.
解答 解:A、氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,碳酸钠能和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠,滴加澄清石灰水时,如果无明显现象,说明氢氧化钠没有变质,如果产生白色沉淀,说明氢氧化钠已经变质;
B、稀盐酸和氯化钡不能反应,稀硫酸和氯化钡反应生成白色沉淀硫酸钡和稀盐酸,利用氯化钡溶液可以区分稀盐酸和稀硫酸;
C、二氧化锰不溶于水,氯化钾易溶于水,通过溶解、过滤、洗涤、干燥可以除去MnO2粉末中的KCl杂质;
D、碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,氯化钠不能和稀盐酸反应,通过滴加稀盐酸不能检验Na2CO3溶液中是否含有NaCl杂质.
故选:D.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
17.下列说法正确的是( )
| A. | 生成盐和水的反应都是中和反应;用含碳酸氢钠的发酵粉焙制糕点 | |
| B. | 服用氢氧化钠治疗胃酸过多;误食重金属盐,可立即服用蛋清或牛奶解毒 | |
| C. | 为人体补充维生素而食用新鲜蔬菜;硒是人体必须的微量元素,应大量服用 | |
| D. | 家用燃气泄漏,立即关闭燃气阀门,开窗透气;干电池可以将化学能转化为电能 |
1.在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水.某课外兴趣小组对生成物中碳的氧化物种类等问题进行了如下探究:
【提示】①CO2+2NaOH═Na2CO3+H2O;②NaOH易溶于水;③浓硫酸能吸水.
【提出问题】生成物中有哪几种碳的氧化物?
【设计实验】兴趣小组同学设计了如下实验:

【实验探究】
(1)观察到A装置(填字母)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成.该装置中发生反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
(2)观察到:①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊;
②E装置中出现红色粉末变成黑色粉末的现象.上述现象都能分别证明草酸分解的气体中含有CO.其中E装置中发生反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
【实验结论】猜测3成立.
【提示】①CO2+2NaOH═Na2CO3+H2O;②NaOH易溶于水;③浓硫酸能吸水.
【提出问题】生成物中有哪几种碳的氧化物?
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | CO和CO2 |

【实验探究】
(1)观察到A装置(填字母)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成.该装置中发生反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
(2)观察到:①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊;
②E装置中出现红色粉末变成黑色粉末的现象.上述现象都能分别证明草酸分解的气体中含有CO.其中E装置中发生反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
【实验结论】猜测3成立.
18.图示“错误操作”与图下面“可能产生的后果”不一致的是( )
| A. | 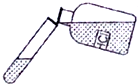 标签被污染 | B. | 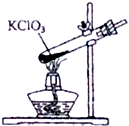 仪器受热不均引起炸裂 | ||
| C. | 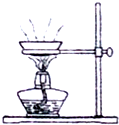 液滴飞溅 | D. | 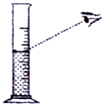 实际值大于读数值 |
16.将一定量的铁粉加入到一定量的硝酸银和硝酸镁的混合液中,充分反应后过滤,向滤渣中加入稀硫酸,有气泡产生,则在滤渣中( )
| A. | 一定有银、铁和镁 | B. | 仅有银和铁 | C. | 可能含镁 | D. | 只有银 |
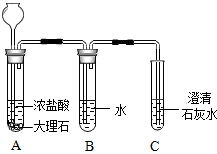 已知盐酸是HCI气体溶于水所形成的溶液,在实验室制取二氧化碳并检验其性质的实验中,如果用浓盐酸代替稀盐酸,并将产生的气体通入澄清的石灰水,往往看不到溶液变浑浊的现象,现有一同学用下列装置进行实验,却看到了澄清石灰水变浑浊的现象.
已知盐酸是HCI气体溶于水所形成的溶液,在实验室制取二氧化碳并检验其性质的实验中,如果用浓盐酸代替稀盐酸,并将产生的气体通入澄清的石灰水,往往看不到溶液变浑浊的现象,现有一同学用下列装置进行实验,却看到了澄清石灰水变浑浊的现象.