题目内容
本题计算必须写过程:
某化学兴趣小组的同学在实验室配制质量分数为20%的碳酸钠溶液,并完成有关实验.
配制100g质量分数为20%的碳酸钠溶液.
配制方法一:需要碳酸钠固体的质量为多少g,水的体积为多少mL(水的密度近似看作1g/cm3).
配制方法二:若用40%的碳酸钠溶液稀释成100克20%碳酸钠溶液,则需取40%的碳酸钠溶液多少亳升?(密度为1.4克/毫升)
【考点】有关溶质质量分数的简单计算.
【专题】溶液的组成及溶质质量分数的计算;有关溶液溶质质量分数的计算.
【分析】根据溶质的质量=溶液的质量×溶质的质量分数,水的质量=溶液的质量﹣溶质的质量,体积=
 ,以及溶液稀释过程中溶质质量不变进行解答.
,以及溶液稀释过程中溶质质量不变进行解答.
【解答】解:配制方法一:需要碳酸钠固体的质量=100g×20%=20g,水的质量100g﹣20g=80g,水的体积=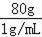
 =80mL;
=80mL;
配制方法二:设40%的碳酸钠溶液的体积为x
100g×20%=40%×x×1.4g/mL
x=35.7mL
故答案为:20;80;35.7mL.
【点评】本题能较好考查学生的思维能力,和分析解决问题的能力,掌握相关知识才能正确分析和解答.

练习册系列答案
相关题目