题目内容
将碳酸钠和氯化钠的固化混合物18.9g,完全溶于100g水中,向其中加入100.8g氯化钡溶液恰好完全反应,过滤,得沉淀的质量为19.7g.
求:(1)原固体混合物中碳酸钠的质量.
(2)反应后所得溶液中溶质的质量分数.
求:(1)原固体混合物中碳酸钠的质量.
(2)反应后所得溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:向碳酸钠和氯化钠组成的混合溶液中加入氯化钡溶液,碳酸钠与氯化钡发生反应生成碳酸钡沉淀和氯化钠,而混合溶液中的氯化钠不与氯化钡反应;至恰好完全反应后,所得溶液为氯化钠溶液,其溶质氯化钠由两部分组成:一部分为原混合物质中的氯化钠,另一部分则是反应生成的氯化钠;
综上所述,所得溶液中溶质质量分数,则是原混合物中氯化钠与生成氯化钠质量总和与所得溶液的质量比.
综上所述,所得溶液中溶质质量分数,则是原混合物中氯化钠与生成氯化钠质量总和与所得溶液的质量比.
解答:解:设固体混合物中Na2CO3的质量为x,生成的NaCl质量为y
Na2CO3+BaCl2═BaCO3↓+2NaCl
106 197 117
X 19.7 y
=
,
=
x=10.6g,y=11.7g
反应后溶液中NaCl的质量分数为:
×100%=10%
答:(1)原固体混合物中碳酸钠的质量10.6g.
(2)反应后所得溶液中溶质的质量分数为10%.
Na2CO3+BaCl2═BaCO3↓+2NaCl
106 197 117
X 19.7 y
| 106 |
| x |
| 197 |
| 19.7g |
| 197 |
| 19.7g |
| 117 |
| y |
x=10.6g,y=11.7g
反应后溶液中NaCl的质量分数为:
| 11.7g+18.9g-10.6g |
| 100.8g+100g+18.9g-19.7g |
答:(1)原固体混合物中碳酸钠的质量10.6g.
(2)反应后所得溶液中溶质的质量分数为10%.
点评:利用质量守恒定律,可以很方便地解决反应后所得溶液的问题:反应后溶液质量=固体混合物质量+溶解所加水的质量+加入氯化钡溶液的质量-生成的沉淀质量.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列安全措施错误的是( )
| A、加油站内及附近要严禁烟火 |
| B、少量天然气泄漏,立即关闭阀门并开窗通风 |
| C、不慎将燃烧着的酒精灯碰倒,立即用湿布覆盖 |
| D、不慎将浓硫酸沾到皮肤上,立即涂上NaHCO3溶液 |
下列各物质的变化中,每一转化在一定条件下均能一步实现的是( )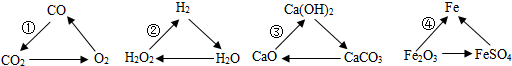

| A、①③④ | B、①③ | C、②③ | D、②④ |
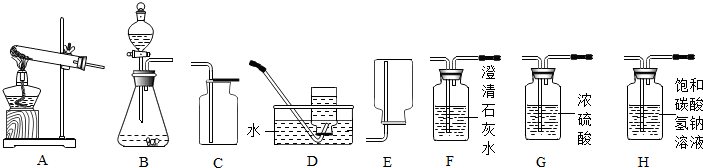
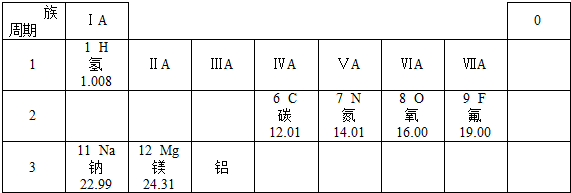
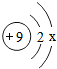 ,其中x为
,其中x为